Академический Документы
Профессиональный Документы
Культура Документы
Apuntes 2 QO2
Загружено:
Amado Hernandez BautistaОригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Apuntes 2 QO2
Загружено:
Amado Hernandez BautistaАвторское право:
Доступные форматы
1
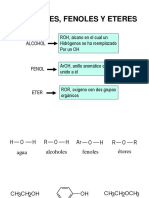
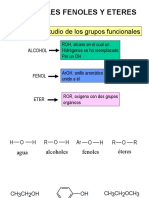
3. Alcoholes
Competencias:
Identificar si se necesita oxidacin o reduccin para interconvertir alcanos, alcoholes, aldehdos, cetonas y cidos, e identificar los reactivos que hacen la conversin. Predecir los productos de las reacciones de alcoholes con agentes oxidantes y reductores, agentes deshidratantes, cidos inorgnicos y cloruros de cido, sodio y potasio. Predecir los productos de las reacciones de iones alcxidos. Indicar como convertir un alcohol en un compuesto semejante con grupos funcionales distintos.
3. Alcoholes
3.1. Reactividad de los alcoholes
3.2. Reacciones de sustitucin de los alcoholes
3.3. Reacciones de eliminacin de los alcoholes 3.4. Oxidacin de los alcoholes 3.5. Uso de los alcoholes en sntesis.
3.1. Reactividad de los alcoholes
Un alcohol puede perder un protn hidroxlico con una base en una reaccin cido-base. El producto es un alcxido.
CH3O-H + Na NH
2
CH3O Na
NH
Los alcoholes pueden desarrollar reacciones de sustitucin en la cual se rompe el enlace CO.
CH3CH2 CH3CH2 OH + HBr
calor
CH3CH2
Br + H 2O
OCH 2CH3 + HI
CH3CH2I + CH 3CH2OH
Los alcoholes, no los teres, desarrollan reacciones de eliminacin para dar calor alquenos.
CH3CH2OH + H2SO4 CH2=CH2 + H 2O
Los alcoholes y los teres no llevan a cabo reacciones de sustitucin o de eliminacin en soluciones alcalinas o neutras. En general, un grupo saliente debe ser una base ms dbil que el nuclefilo atacante. Los grupos OH y OR son bases fuertes y entonces grupos salientes muy pobres. Las reacciones de sustitucin y eliminacin de alcoholes proceden en solucin cida.
3.2. Reacciones de sustitucin de los alcoholes
En solucin cida, el grupo OH de un alcohol est protonado. Aunque el OH es un grupo saliente pobre, el nuevo grupo OH2+, es un buen grupo saliente, porque es una base muy dbil.
R OH R OH H
Nu
Nu + H 2O
buen grupo saliente
En las reacciones de sustitucin de alcoholes los reactivos ms tiles son los HX. El producto de la reaccin de un alcohol con HX es un RX.
Reactividad de halogenuros de hidrgeno De los HX, el cido ms fuerte es HI, le sigue el HBr, luego el HCl y el cido ms dbil es HF. La velocidad de las reacciones sigue el mismo orden: ms rpidas con HI y menos con HCl. Reactividad de alcoholes Todos los alcoholes desarrollan reaccin con HBr y HI fcilmente para dar RBr y RI. Los alcoholes terciarios reaccionan fcilmente con HCl. Sin embargo, alcoholes 1 y 2 son menos reactivos y requieren ZnCl2 para reaccionar con HCl. Los alcoholes 2 y 3 desarrollan reaccin con HX por SN1 y los 1 por SN2.
3.3. Reacciones de eliminacin de los alcoholes
Los alcoholes realizan reacciones de eliminacin para dar alquenos. Debido a que esta reaccin se lleva a cabo con prdida de agua, se conoce como de deshidratacin. 60 C (CH3)2C=CH2 + H 2O (CH3)3COH + H2SO4
Los ROH 1 requieren de mayor temperatura para reaccionar (180 C). Para ROH 2 y 3, la deshidratacin sigue el mecanismo E1. El grupo OH es protonado, se forma el carbocatin, y luego un protn es eliminado para dar el alqueno. Si existe la posibilidad de que se forme ms de un alqueno, se producir el alqueno ms sustitudo, el ms estable (regla de Saytseff).
OH2
Etapa 1
CH3-CH-CH3 H
CH3-CH-CH3
H
Etapa 2
CH3-CH-CH2
CH3CH=CH2
Como las reacciones de deshidratacin de ROH 2 y 3 implican carbocationes, los rearreglos pueden ocurrir. La deshidratacin de R-OH no es un buen mtodo para preparar un alqueno. Es preferible convertir un alcohol a un RX y someter el RX a una eliminacin E2.
3.4. Oxidacin de los alcoholes
En qumica inorgnica, se define la oxidacin de un tomo como prdida de electrones, mientras que reduccin es la ganancia de electrones por un tomo. En qumica orgnica, si una molcula gana oxgeno o pierde hidrgeno, se oxida. Si una molcula pierde oxgeno o gana hidrgeno, se reduce. Los alcoholes puden ser oxidados a cetonas, aldehdos o cidos carboxlicos. Estas oxidaciones son usadas ampliamente en el laboratorio y en la industria, y tambin ocurren en sistemas biolgicos.
O
[O]
R-CH
aldehdo alcohol 2
OH
[O]
O R-C-R
cetona
alcohol 1 RCH OH 2
[O]
R-CH-R
RCOOH
cido carboxlico
Combustin de etanol
Los alcoholes, como otros compuestos orgnicos, llevan a cabo combustin, produciendo CO2 y agua.
Oxidacin biolgica del etanol
En los mamferos, el alcohol tomado es oxidado primero en el hgado con la ayuda de una enzima llamada alcohol deshidrogenasa. El producto de esta deshidrogenacin es el acetaldehdo, CH3CHO. Este acetaldehdo es despus oxidado enzimticamente al in acetato, CH3CO2 , el cual despus se esterifica con el tiol coenzima A. El producto de la esterificacin es acetilcoenzima A. El grupo acetilo en la acetilcoenzima A puede convertirse en CO2, agua y energa, o puede convertirse en otros compuestos, como grasa.
alcohol deshidrogenasa
O
[O]
O CH3COO
HSCoA
CO2 + H 2O
CH3CH2OH
CH3-CH
CH3-C-SCoA
NH2 N
grasa
CH3
O O-PO CH2 O N N
CH3CS-CH2CH2NHCOCH2CH2NHCOCHCCH2OP OHCH3
OH HO OH
acetilcoenzima A
OPO3H
Oxidacin de alcoholes en el laboratorio
Los agentes oxidantes de laboratorio oxidan alcoholes primarios a cidos carboxlicos y alcoholes secundarios a cetonas. Algunos agentes oxidantes tpicos son: (1) KMnO4 alcalino (2) HNO3 concentrado, caliente (3) H2CrO4 (preparado in situ de CrO3 o Na2CrO4 con H2SO4) Los alcoholes primarios se oxidan primero a aldehdos. Los aldehdos son ms fciles de oxidar que los alcoholes; por lo que la oxidacin contina hasta que se forme el cido carboxlico (o en soln alcalina, el anin).
O CH3CH2CH2OH + H 2CrO4
H
CH3CH2-CH
CH3CH2CO2H
+ Cr 3+
_
CH2OH + MnO 4
OH
CHO
CO2 +
MnO 2
El mejor reactivo para oxidar un alcohol primario a aldehdo es un complejo xido crmicopiridina, el cual no oxida el aldehdo a cido carboxlico.
CO2H
Oxidacin de alcoholes en el laboratorio
Los alcoholes secundarios son oxidados a cetonas con buenos rendimientos por agentes oxidantes normales.
OH + KMnO 4
OH
Los alcoholes terciarios no se oxidan bajo condiciones alcalinas. Si la oxidacin se coloca en solucin cida, el alcohol terciario se deshidrata y entonces el alqueno se oxida.
no hay reaccin
[O]
R2CHOH
H
OH
[O]
alquenos
productos de oxidacin de alquenos
10
3.5. Uso de los alcoholes y teres en sntesis.
Los alcoholes son materias primas verstiles para la preparacin de halogenuros de alquilo, alquenos, compuestos carbonlicos y teres.
RX
PX3 HX TsCl
) RX ( posible re arre glo
ROTs
RX o alqueno
ROH
H2SO4 [O] R'COOH' Na o K
alqueno ( posible re arre glo )
cetona, aldehdo, o cido carboxlico
RCOOR'
un ste r
RO
R'X
ROR'
un te r
11
4. Alquenos
Competencias:
Predecir los productos de adiciones, oxidaciones, reducciones y rupturas de alquenos, incluyendo la orientacin de la reaccin y la estereoqumica.
Proponer mecanismos lgicos para explicar los productos observados de las reacciones de alquenos, incluyendo su regioqumica y estereoqumica.
12
4. Alquenos
4.1. Adicin de halogenuros de hidrgeno a alquenos
4.2. Adicin de H2SO4 y H2O a alquenos
4.3. Adicin de borano a alquenos 4.4. Adicin de halgenos a alquenos 4.5. Hidrogenacin cataltica 4.6. Oxidacin de alquenos
4.7. Uso de alquenos en sntesis.
13
4. Alquenos
Las 3 reacciones tpicas de alquenos son las reacciones con hidrgeno, con cloro y con halogenuro de hidrgeno.
H2 / Pt Cl2 HCl
CH3CH3 Cl H2C Cl CH2
CH2=CH2
CH3CH2Cl
Cada una de estas reacciones es una reaccin de adicin. En cada caso el reactivo se agrega al alqueno sin que se pierda algn tomo. La principal caracterstica de los compuestos insaturados es la adicin de reactivos a los enlaces pi. En estas reacciones, el enlace pi se rompe y su par de electrones se usa en la formacin de dos nuevos enlaces sigma. Los compuestos con enlaces pi son de mayor energa que los compuestos parecidos con solamente enlaces sigma, por lo que las reacciones de adicin son generalmente exotrmicas.
14
4.1. Adicin de halogenuros de hidrgeno a alquenos
Los HX se adicionan a los enlaces pi de los alquenos para producir RX. La reactividad relativa de HX en esta reaccin es HI > HBr > HCl > HF. Un HX contiene un enlace altamente polar y puede ceder H+ al enlace pi de un alqueno.
El mecanismo es mediante el ataque del protn para dar un carbocatin intermediario, que reacciona rpidamente con el halogenuro para dar el RX (adicin electroflica).
H Cl H CH3CHCHCH3 + Cl
Carbocatin intermediario
Etapa 1 (lenta)
CH3CH=CHCH3
Cl
Etapa 2 (rpida)
CH3CHCH2CH3
+ Cl
CH3CHCH2CH3
15
4.1. Adicin de halogenuros de hidrgeno a alquenos
Regla de Markovnikov (qumico ruso Vladimir Markovnikov, 1869) Si un alqueno es asimtrico, se pueden formar 2 productos diferentes con la adicin de HX. En las adiciones de HX a alquenos asimtricos, el H+ del HX se une al carbono del doble enlace que ya tenga el mayor nmero de hidrgenos.
el H se une aqu
Cl
HCl
La razn de la regla de Markovnikov La adicin de un reactivo a un alqueno asimtrico procede a travs de un carbocatin ms estable.
16
4.1. Adicin de halogenuros de hidrgeno a alquenos
Adicin anti-Markovnikov de HBr
La adicin de HBr a los alquenos a veces no cumple este regla. Esto no ocurre con HCl o con HI. El oxgeno es un bi-radical estable y los perxidos (ROOR) se rompen fcilmente dando radicales libres. Cuando estn presentes O2 o perxidos, la adicin de HBr procede a travs de un mecanismo por radicales libres, en lugar de un mecanismo inico.
Radical libre ms estable
17
4.2. Adicin de H2SO4 y H2O a alquenos
El cido sulfrico lleva a cabo adicin a un alqueno al igual que un HX. El producto es un sulfato de alquilo, til para preparar alcoholes y teres.
OSO3H CH3CH=CH2 + H-OSO 3H CH3CH-CH3
hidrgeno sulfato de 2-propilo
Si una traza de cido fuerte, est presente como catalizador, el agua tambin se adiciona al doble enlace para dar un alcohol (hidratacin de un alqueno).
OH CH3CH=CH2 + H 2O CH3CH-CH3
En ambas reacciones, el primer paso es la protonacin del alqueno para producir un carbocatin.
El 2 paso es la adicin de un nuclefilo al carbocatin. Siguen la regla de Markovnikov y rearreglos si es necesario.
18
4.3. Adicin de borano a alquenos
El diborano (B2H6), disuelto en ter etlico se disocia en borano (BH3). Si el borano se adiciona a un doble enlace, el in hidruro se une al tomo de carbono ms sustituido (anti-Markovnikov).
El H sobre el carbono ms sustituido
Los organoboranos se oxidan a alcoholes, con perxido de hidrgeno alcalino. Los rendimientos globales son 95-100%.
OH
CH3
(1) BH3 (2) H2O2, -OH
CH3
Cuando el borano se adiciona a un doble enlace, el tomo de boro y el ion hidruro se unen simultneamente a los dos tomos de carbono del doble enlace (adicin cis o sin).
19
4.4. Adicin de halgenos a alquenos
El cloro y el bromo se adicionan a C=C. Una prueba comn de laboratorio para dobles y triples enlaces en un compuesto de estructura desconocida es el tratamiento con una soln diluda de bromo en CCl4. El reactivo tiene un color caf rojizo que desaparece si la prueba es positiva (las cetonas y fenoles tambien decoloran la soln Br2/CCl4 ).
Br Br CH3CH=CHCH3 + Br 2
2-buteno rojo
CH3CH-CHCH3
2,3-dibromobutano (sin color)
Esta reaccin de adicin es general slo para cloro y bromo. Un alqueno ms sustituido es ms reactivo hacia X2 que un alqueno menos sustituido, en el mismo orden de reactividad que hacia HX.
20
4.4. Adicin de halgenos a alquenos
A) Ataque electroflico de X2
Cuando X2 se aproxima a los electrones del enlace pi, se induce la polaridad en la molcula de X2 por la repulsin entre electrones pi y los electrones de la molcula de X2 . Conforme el enlace X-X se polariza se hace ms dbil hasta que se rompe. El resultado es un ion organohalogenado, llamado ion halonio.
Br CH2=CH2 Br + Br - Br
CH2- CH2
Si el alqueno no es simtrico, el bromo con la carga positiva es llevado sobre el carbono ms sustituido.
21
B) anti-ataque de XEl ion intermedio puenteado est cargado positivamente y es de alta energa. La reaccin se completa con el ataque de un nuclefilo. Un Br- cargado negativamente no puede atacar al carbono del intermedario puenteado por la parte de arriba (como en el dibujo); entonces el Br- ataca del lado opuesto del intermediario. El resultado es una anti-adicin de Br2 al doble enlace. d+
Br H H3C
d+
H3C H H Br Br
Br
C) Evidencia para la adicin anti
trans-1,2-dibromociclohexano
22
D) Adicin mixta
En el caso de la reaccin de bromacin, llevada a cabo con Br2 en una solucin que contiene Cl-. En esta reaccin hay dos nuclefilos, por lo que se observan productos dihalogenuros mixtos (dibromoalcano y algo de bromo-cloro-alcano).
E) Adicin de halgenos y agua
Cuando un alqueno se trata con una mezcla de Cl2 o Br2 en agua, se forma una 1,2-halohidrina.
1,2-halohidrina
23
4.5. Hidrogenacin cataltica
La adicin cataltica de gas hidrgeno a un alqueno es una reduccin de compuestos con enlace pi.
CH3CH=CH2 + H 2
Pt
CH3CH2CH3
Las reacciones de hidrogenacin son exotrmicas, pero no proceden de manera espontnea porque sus Eact son muy altas. Como catalizador se usa un metal finamente dividido o un metal adsorbido en un soporte inerte (carbn). El platino, el paladio y el nquel son los catalizadores tpicos.
Los 2 hidrgenos se adicionan del mismo lado del doble enlace (adicin sin). Si los productos de hidrogenacin pueden dar lugar a isomerismo geomtrico, el producto cis- es el predominante.
24
4.6. Oxidacin de alquenos
1. Oxidacin del enlace pi sin ruptura del enlace sigma, y 2. Oxidacin del enlace pi con ruptura del enlace sigma.
OXIDACIN SIN RUPTURA
KMnO4 con OH (fro) OsO4 seguido de Na2SO3 C6H5CO3H
1,2-dioles (glicoles) 1,2-dioles (glicoles) epxidos cidos carboxlicos y cetonas cidos carboxlicos y cetonas aldehdos y cetona
OXIDACIN CON RUPTURA
KMnO4 (caliente) O3 seguido de H2O2 con H+ O3 seguido de Zn con H+
25
4.6. Oxidacin de alquenos
El reactivo ms usado para convertir un alqueno en un glicol, es una solucin fra, alcalina, de KMnO4 (prueba de Baeyer). El tetraxido de osmio da mejores rendimientos de glicoles, pero su uso es limitado por su toxicidad.
H OsO 4 H O O Os O O Na 2SO3 H
H + Os OH OH
cis-
26
El tratamiento de un alqueno con cido perbenzoico en un solvente inerte produce un epxido. O O
O CH3CH=CHCH3 + COOH H3C CH 3 + COH
Esta reaccin conduce a trans-1,2-dioles
Oxidacin con ruptura
Los productos de oxidacin con ruptura dependen tanto de las condiciones de oxidacin como de la estructura del alqueno. Si los carbonos de la doble ligadura del alqueno no tienen hidrgenos, el rompimiento por oxidacin producir 2 cetonas. Si los carbonos de la doble ligadura del alqueno tienen un hidrgeno, el rompimiento por oxidacin producir aldehdo o cido carboxlico, dependiendo de las condiciones de reaccin.
27
Ruptura con KMnO4
Una soln caliente de KMnO4 es una vigoroso agente oxidante que lleva a solamente cetonas y cidos carboxlicos.
Ozonlisis
La ozonlisis consiste en 2 reacciones separadas: (1) oxidacin del alqueno a un oznido, y (2) tanto la reduccin u oxidacin del oznido a los productos finales. En la oxidacin inicial se burbujea ozono a travs de la solucin del alqueno con un solvente inerte (CCl4). El ozono ataca el enlace pi para dar un intermediario inestable llamado 1,2,3-trioxolano. De la ruptura O O del enlace sigma se obtiene un oznido.
Zn
O
O3
H+,H2O
+
H O O
H2O2 H
+
+
OH
Вам также может понравиться
- 10 Alcoholes y FenolesДокумент23 страницы10 Alcoholes y Fenolesrojo100% (1)
- Solucionario Química Chang (Capítulo II - 10 Edición)Документ35 страницSolucionario Química Chang (Capítulo II - 10 Edición)Eliud Ulises Aguilar Durán100% (2)
- Clase - I - Alcoholes 1Документ35 страницClase - I - Alcoholes 1joseОценок пока нет
- Reacciones de Los AlcoholesДокумент15 страницReacciones de Los Alcoholesbernardo antonio barralОценок пока нет
- Informe Identificación de AlcoholesДокумент10 страницInforme Identificación de AlcoholesCristianDavidVilladaОценок пока нет
- Practica 3Документ7 страницPractica 3Alfonso Guadalupe Cacho AguirreОценок пока нет
- Practica de Laboratorio 8Документ17 страницPractica de Laboratorio 8ALDO CLEOCEL CURASMA LUCASОценок пока нет
- AlcoholesДокумент5 страницAlcoholesfarfan. julio CortezОценок пока нет
- Alcoholes y TiolesДокумент67 страницAlcoholes y TiolesGisseli QG100% (1)
- Lección N5. Q.O. Funciones Químicas OxigenadasДокумент68 страницLección N5. Q.O. Funciones Químicas OxigenadaswaldirОценок пока нет
- Reacciones de Alcoholes y FenolesДокумент58 страницReacciones de Alcoholes y FenolesRODRIGO DE JESUS RUBIO ROSASОценок пока нет
- Reacciones Redox en OrganicaДокумент25 страницReacciones Redox en OrganicaMarianet ZereneОценок пока нет
- PruebasДокумент14 страницPruebasEdinson CaicedoОценок пока нет
- Sustitucion Nucleofilica Grupo CarboniloДокумент28 страницSustitucion Nucleofilica Grupo CarbonilosemperprogrediОценок пока нет
- Alcohol EsДокумент28 страницAlcohol EsElizabeth EscalanteОценок пока нет
- Boletin 5Документ15 страницBoletin 5Jonathan AgueroОценок пока нет
- AlcoholesДокумент12 страницAlcoholesAndy LezametaОценок пока нет
- Alcoholes 2009-1Документ58 страницAlcoholes 2009-1Alison RoaОценок пока нет
- Trabajo QuimicaДокумент31 страницаTrabajo Quimicalina maria icopo poloОценок пока нет
- Clase - I - Alcoholes 2Документ22 страницыClase - I - Alcoholes 2Yuber DiazОценок пока нет
- Alcoholes Informe "VISITEN MI BLOG ALLÍ ESTOY SUBIENDO NUEVOS ARCHIVOS Http://quimicofiq - Blogspot.com/"Документ10 страницAlcoholes Informe "VISITEN MI BLOG ALLÍ ESTOY SUBIENDO NUEVOS ARCHIVOS Http://quimicofiq - Blogspot.com/"denis100% (52)
- 10 Alcoholes y FenolesДокумент23 страницы10 Alcoholes y Fenolesalmine rojas0% (1)
- QUIMICA ORGANICA PAU - Apuntes - Ejercicios PDFДокумент11 страницQUIMICA ORGANICA PAU - Apuntes - Ejercicios PDFPere Egolatra AlterОценок пока нет
- II-2 Sintesis de Los Alcoholes 202310Документ47 страницII-2 Sintesis de Los Alcoholes 202310Andrés Solís GonzálezОценок пока нет
- Alcohol EsДокумент20 страницAlcohol EsjanssenОценок пока нет
- Funciones Orgánicas OxigenadasДокумент11 страницFunciones Orgánicas Oxigenadaskatizita07100% (2)
- Compuestos Oxigenados AlcoholesДокумент23 страницыCompuestos Oxigenados AlcoholesStiven PiñeirosОценок пока нет
- Funciones Organicas OxigenadasДокумент11 страницFunciones Organicas OxigenadasAlfredo FernandezОценок пока нет
- Aldehidos y Cetonas CLASEДокумент28 страницAldehidos y Cetonas CLASEMarianellaTellezLazaroОценок пока нет
- Alcoholes 1Документ34 страницыAlcoholes 1Raul CabreraОценок пока нет
- Reducción de Enlaces Múltiples C - CДокумент12 страницReducción de Enlaces Múltiples C - CSilvia Rivera SivilaОценок пока нет
- Alquenos (Completo)Документ5 страницAlquenos (Completo)Maria WinogradОценок пока нет
- Alcoholes, Expo de QuimicaДокумент30 страницAlcoholes, Expo de QuimicaVIERHITG HOSHUA ACEVEDO LAVALLEОценок пока нет
- Alcoholes QuimicaДокумент12 страницAlcoholes QuimicaRoberto CarlosОценок пока нет
- Taller 7.1 Alcoholes PDFДокумент7 страницTaller 7.1 Alcoholes PDFEli Yuqui VillacresОценок пока нет
- Reacciones de Los Alcoholes, Fenoles y ÉteresДокумент6 страницReacciones de Los Alcoholes, Fenoles y ÉteresBelen Rocio Delmar Flores CaribauxОценок пока нет
- Reacciones de SustitucionДокумент10 страницReacciones de SustitucionSagrario AltamiraОценок пока нет
- Alcoholes y Fenoles Acidos Carboxilicos y DerivadosДокумент51 страницаAlcoholes y Fenoles Acidos Carboxilicos y DerivadoskevinОценок пока нет
- Labo AlcoholesДокумент6 страницLabo AlcoholesJuan Carlos VargasОценок пока нет
- Informe de Lab de Quimica N 05 Alcoholes TerminadoДокумент41 страницаInforme de Lab de Quimica N 05 Alcoholes TerminadoLuis Javier Alva100% (1)
- Alcohol EsДокумент31 страницаAlcohol EsGuillermo Saldaña TorresОценок пока нет
- Organica 7Документ27 страницOrganica 7Cochachin Espinoza Hector FelixОценок пока нет
- Preparación de Haluros de AlquiloДокумент17 страницPreparación de Haluros de AlquiloBallesteros AndresОценок пока нет
- Reacciones de Los AlcoholesДокумент7 страницReacciones de Los Alcoholessofia pontilloОценок пока нет
- Practica 3Документ17 страницPractica 3mike rdzОценок пока нет
- Oxidación de Alcanos Alquenos y AlquinosДокумент15 страницOxidación de Alcanos Alquenos y AlquinosWilbert Rivera Muñoz60% (5)
- Reacciones de Los AlcoholesДокумент7 страницReacciones de Los AlcoholesMiguel Angel Ramos PerezОценок пока нет
- Tema 1 - 2 Ac. CarboxilicosДокумент32 страницыTema 1 - 2 Ac. CarboxilicosHoracio GorosteguiОценок пока нет
- Unidad 4. Compuestos Oxigenados 1Документ42 страницыUnidad 4. Compuestos Oxigenados 1Blanca Mariela Ccari CuentaОценок пока нет
- Unidad IV Acidos Carboxilicos y DerivadosДокумент54 страницыUnidad IV Acidos Carboxilicos y DerivadosLyn Xajil0% (1)
- Guia 5 Reconocimiento Alcoholes Aldehidos CetonaДокумент6 страницGuia 5 Reconocimiento Alcoholes Aldehidos CetonaDanielpsebastianОценок пока нет
- Reacciones de Los Hidrocarburos AlifáticosДокумент53 страницыReacciones de Los Hidrocarburos Alifáticosdaniela morenoОценок пока нет
- CAPÍTULO 17 Aldehidos y CetonasДокумент21 страницаCAPÍTULO 17 Aldehidos y Cetonasmadrenaturaleza100% (2)
- Alcoholes 3Документ22 страницыAlcoholes 3jorge luis villanuevaОценок пока нет
- Química Orgánica Unidad 2Документ24 страницыQuímica Orgánica Unidad 2Amalfy Lised Cubillos Huaca100% (1)
- Acidos Bases NuevoДокумент27 страницAcidos Bases NuevoJuanNietoSantosОценок пока нет
- 1BtoProfesorActividadesQuimica3Eva PDFДокумент14 страниц1BtoProfesorActividadesQuimica3Eva PDFmusic MúsicaОценок пока нет
- Quimica Domingo 12.03.2023Документ4 страницыQuimica Domingo 12.03.2023trygpt213Оценок пока нет
- Guia 5 Sexto Grado Opaz DistanciaДокумент3 страницыGuia 5 Sexto Grado Opaz DistanciaBoris Enrique MezaОценок пока нет
- Ieee 525 PDFДокумент19 страницIeee 525 PDFZacarias RomeroОценок пока нет
- Alacalinos y AlcalinoterreosДокумент3 страницыAlacalinos y AlcalinoterreosTahyri ShicayОценок пока нет
- La Composición Química de Los Seres VivosДокумент1 страницаLa Composición Química de Los Seres VivosElvira D. Padilla NarváezОценок пока нет
- Observaciones Informe TP N°4 QIДокумент6 страницObservaciones Informe TP N°4 QIT tОценок пока нет
- Q0 PAU EstequiometríaДокумент8 страницQ0 PAU EstequiometríacampolatorcaОценок пока нет
- Actividad 8Документ4 страницыActividad 8Jack ProОценок пока нет
- Presentación Proceso Bayer LADO ROJOДокумент81 страницаPresentación Proceso Bayer LADO ROJOpedro garciaОценок пока нет
- Aleaciones de Metales No FerrososДокумент7 страницAleaciones de Metales No FerrososTomas Castro D SantosОценок пока нет
- Casos de Estudio 2 Quimica GeneralДокумент3 страницыCasos de Estudio 2 Quimica GeneralFranko Pacheco PerezОценок пока нет
- SERIE #5 y 6 Año 2020Документ6 страницSERIE #5 y 6 Año 2020Mauricio AcostaОценок пока нет
- Alcohol EsДокумент20 страницAlcohol EsjanssenОценок пока нет
- Practica #4 TerminadoДокумент6 страницPractica #4 Terminadomarco antonioОценок пока нет
- Taller AireДокумент4 страницыTaller AireJaylette MejiaОценок пока нет
- Curvas de TitulaciónДокумент11 страницCurvas de TitulaciónDaniela ClavijoОценок пока нет
- Marco Teorico Laboratorio 5Документ12 страницMarco Teorico Laboratorio 5María FernandaОценок пока нет
- Manual de Calderas PDFДокумент24 страницыManual de Calderas PDFTabitha ThompsonОценок пока нет
- Cianuro de Sodio CIANURO DE SODIOДокумент8 страницCianuro de Sodio CIANURO DE SODIOMaykolFabreOrtОценок пока нет
- Codex Agua Mineral NaturalДокумент4 страницыCodex Agua Mineral NaturalJaime Santisteban CáceresОценок пока нет
- Evaluacion de QuimicaДокумент4 страницыEvaluacion de Quimicamprm2579Оценок пока нет
- Taller 2 Química GeneralДокумент4 страницыTaller 2 Química GeneralDaniela Hernandez AmayaОценок пока нет
- Cables RTD PDFДокумент4 страницыCables RTD PDFjavier perezОценок пока нет
- Norma Tecnica Guatemalteca 29001 Agua Potable - ConguanorДокумент13 страницNorma Tecnica Guatemalteca 29001 Agua Potable - ConguanorCarlos A. MendezОценок пока нет
- Tinto Introduccion Ejercicios Descrude Blanqueo Teñido (V)Документ28 страницTinto Introduccion Ejercicios Descrude Blanqueo Teñido (V)Mar Cerda SilvaОценок пока нет
- Quimica Composicion Centesimal MariaДокумент2 страницыQuimica Composicion Centesimal Mariafelixdavidleiva6520Оценок пока нет
- Curio y NeptunioДокумент11 страницCurio y NeptunioJaz AragonОценок пока нет