Академический Документы
Профессиональный Документы
Культура Документы
ENZIMOLOGIA
Загружено:
Miguel Angel100%(1)100% нашли этот документ полезным (1 голос)
211 просмотров22 страницыОригинальное название
ENZIMOLOGIA.ppt
Авторское право
© © All Rights Reserved
Доступные форматы
PPT, PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате PPT, PDF, TXT или читайте онлайн в Scribd
100%(1)100% нашли этот документ полезным (1 голос)
211 просмотров22 страницыENZIMOLOGIA
Загружено:
Miguel AngelАвторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате PPT, PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 22
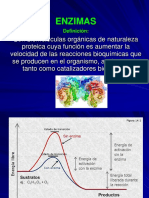
ENZIMAS
W. BENJAMIN RUIZ CHANG
MAGISTER EN BIOQUIMICA
PROFESOR AUXILIAR - UPAO
Las enzimas son biocatalizadores excelentes, mas eficaces y especficos que dirigen y
regulan reacciones de los sistemas biolgicos.
Todas las enzimas tienen las siguientes propiedades qumicas:
* Aumentan la velocidad de una reaccin al disminuir la energa de activacin.
* No se consume ni sufre cambios en sus estructura durante el proceso cataltico.
* Acta sobre una molcula orgnica denominada sustrato, transformndola en un
producto o productos.
* Son reguladas por una gran variedad de controles celulares, genticos y alostricos.
ENZIMAS
Catalizan reacciones de transferencia de electrones y/o protones de un sustrato a otro; es
decir reacciones de oxido-reduccin.
- * Deshidrogenasas * Oxidasas * Oxigenasas
- * Reductasas * Peroxidasas * Hidroxilasas
CLASIFICACION ENZIMATICA
LACTATO
DESHIDROGENASA
CLASE 1: OXIDORREDUCTASAS
LACTATO PIRUVATO
Catalizan la transferencia de un grupos funcionales entre donadores y aceptores.
Los grupos que son transferidos frecuentemente son: fosfato, amino, glucosilo.
* Quinasas * Transaminasas * Transmetilasas
CLASE 2: TRANSFERASAS
GLUCOCINASA
GLUCOSA ADENOSIN TRIFOSFATO
GLUCOSA-6-FOSFATO ADENOSIN DIFOSFATO
CLASE 3: HIDROLASAS
Estas reacciones implican la ruptura hidroltica
de enlaces C-O, C-N, O-P y C-S.
Se les puede considerar como como una clase
especial de transferasas en las que el sustrato
es escindido siendo sus fragmentos transferidos a
los componentes del agua (OH y H).
* Lipasas * Esterasas
* Glucosidasas * Peptidasas
LACTASA
LIPASA
TRIGLICERIDO
CIDOS GRASOS LIBRES GLICEROL
LACTOSA
GLUCOSA
GALACTOSA
CLASE 4: LIASAS
Catalizan reacciones en la que se rompen enlaces C-C, C-N y C-O, sin intervencin de
agua y con prdida de grupos funcionales simultnea a la aparicin de dobles enlaces.
* Descarboxilasas * Desaminasas
Catalizan reacciones de isomerizacion de cualquier tipo, pticos, geomtricos o de posicin.
* Epimerasa * Racemasa * Mutasa
CLASE 5: ISOMERASAS
PIRUVATO
DESCARBOXILASA
ALANINA
RACEMASA
PIRUVATO
ACETALDEHIDO
DIOXIDO DE
CARBONO
L-ALANINA
D-ALANINA
CLASE 6: LIGASAS
Participan en reacciones en las que se unen
dos molculas a expensas de un enlace
fosfato de alta energa procedente del ATP.
El termino sintetasa se reserva para este
grupo de enzimas.
* Tiocinasa * Sintetasa
CITRATO
SINTASA
Oxalacetato Citrato
GLUTAMINA
SINTETASA
GLUTAMATO
GLUTAMINA
NATURALEZA QUIMICA DE LAS ENZIMAS
La mayora de las enzimas (Apoenzimas)
son de naturaleza proteica (90%).
Algunas enzimas requieren de un
componente adicional (cofactor o coenzima)
para su funcionamiento. Estos se unen por
medio de enlaces dbiles no covalentes.
Las Coenzimas son molculas orgnicas,
generalmente derivan de las vitaminas (NAD,
FAD, Biotina, Tiamina).
Los Cofactores son iones inorgnicos (Mg
+2
,
Cu
+2
, Fe
+2
, Zn
+2
).
Cofactor
Apoenzima
HOLOENZIMA
ENZIMA
SUSTRATO
OXIDADO
NADH
SUSTRATO
REDUCIDO
NAD
ENZIMA
COMPLEJO
ENZIMA-SUSTRATO
+
+ +
Coenzima
Enzima
(sacarasa)
Sitio
cataltico
1
2
3
Sustrato
(sacarosa)
Enzima disponible con
sitio ctaltico vaco
Sustrato se une a
la enzima por
encaje inducido
Sustrato es
convertido a
productos
4
Productos son
liberados
Glucosa Fructosa
SITIO CATALITICO
El sitio cataltico o centro de fijacin del
sustrato, es una pequea grieta o hendidura en
una molcula proteica grande, donde se fija el
sustrato.
La estructura terciaria de la enzima est
plegada de tal manera que se origina una
regin con las dimensiones moleculares
idneas para acomodar un sustrato especfico.
sitio cataltico de
carboxipeptidasa
La especificidad reside en una regin
determinada de la superficie enzimtica, el
centro de fijacin del sustrato.
Pueden presentar especificidad ptica
absoluta para al menos, una porcin de la
molcula del sustrato o a la totalidad de
dicha molcula.
ESPECIFICIDAD DE LAS ENZIMAS
ISOENZIMAS
Son enzimas que tienen diferente
secuencia de aminocidos, es
decir, son formas moleculares
diferentes. pero catalizan la misma
reaccin qumica.
Estas isoformas son codificadas por
genes diferentes y sintetizados en
tejidos diferentes.
Su accin la realizan de forma
intracelular, es decir a nivel del
citoplasma de las clulas.
ISOENZIMAS DE CREATINA FOSFOQUINASA
ISOENZIMAS DE LACTATO DESHIDROGENASA
ELECTROFORESIS
DENSITOGRAMA
Ribozimas.- son RNAs catalticos, estn
constituidos por nucletidos, son
importantes en la eliminacin de intrones
y ensamblaje de exones, es decir en el
mecanismo de maduracin del RNA
Abzimas.- son anticuerpos catalticos de
naturaleza proteica del tipo de las
inmunoglobulinas (Ig), sirven como
molculas de proteccin neutralizando
sustancias extraas de daan las clulas.
Sinsimas.- son enzimas de origen
sinttico, se utilizan para el tratamiento
de enfermedades, como las adicciones a
drogas.
Granzimas.- son proteasas que inducen
o activan procesos de apoptosis, se
sintetizan como zimgenos y se activan
en lugares especficos de la clula.
Apoptosis
Clula normal
Clula modificada
Gen
pre RNAm
RNA maduro
Transcripcin
Maduracin
MODELOS ENZIMTICOS
MODELO DE LLAVE Y CERRADURA
(E. Fischer).
El sitio cataltico es una estructura
rgida, por lo tanto el sustrato y la
enzima se acoplan de forma
estereoespecfica, de la misma manera
que una llave se ajusta a su cerradura.
MODELO DEL AJUSTE INDUCIDO
(D. Koshland).
El sitio cataltico es una estructura
dotada de flexibilidad, cuando el sustrato
se une a la enzima, induce cambios
conformacionales en esta molcula, para
asegurar la ubicacin ms efectiva.
FACTORES QUE MODIFICAN LA ACTIVIDAD ENZIMTICA
CONCENTRACIN DEL SUSTRATO
Cuando aumenta la concentracin de sustrato, se produce un aumento en la velocidad
de reaccin, al seguir aumentando la concentracin de sustrato la velocidad de reaccin
se hace constante. Por lo tanto obtiene una velocidad mxima de reaccin.
Esto nos sirve para obtener la velocidad mxima media, y por ende determinar el Km de
la reaccin (constante de Michaelis-Menten)
L
Km = Afinidad
EFECTO DE LA TEMPERATURA
En organismos vegetales la temperatura optima esta entre 20 a 37C promedio,
cuando disminuye o aumenta esta temperatura la actividad enzimatica disminuye, la
enzima sufre alteraciones en su estructura.
Por debajo de la temperatura promedio la actividad de la enzima disminuye por que
esta sufre un proceso de inactivacion (proceso reversible), pero si la temperatura
aumenta por encima de la optima la actividad enzimatica tambien disminuye, pero a
diferencia de la primera la enzima sufre un proceso de desnaturalizacin (proceso
irreversible).
Temperatura ptima para
enzima de termfila
A
c
t
i
v
i
d
a
d
0 20 40 80 100
Temperatura (C)
Temperatura ptima para dos enzimas
Temperatura ptima para una
tpica enzima humana
EFECTO DEL PH
La mayoria de las enzimas tiene un pH ptimo
que varia entre 6-8. Pero tambien va a
depender del tejido o del organo para poder
determinar el pH mas optimo para las
enzimas. Los cambios de pH en el medio
pueden afectar el estado de ionizacin de
ciertos grupos funcionales en la enzima y
tambin en la del sustrato.
Tanto la disminucion, como el aumento del
pH, afectan la actividad enzimatica por que
producen la desnaturalizacion de la enzima.
ENZIMA pH
Fosfatasa alcalina 9.5
Lipasa 8.0
Quimotripsina 8.0
Tripsina 7.9
Catalasa 7.6
Carboxipeptidasa 7.5
Amilasa 6.8
Fosfatasa cida 5.0
Pepsina 1.5
A
c
t
i
v
i
d
a
d
pH ptimo para dos enzimas
pH ptimo para pepsina
pH ptimo para
tripsina
1
0 2 3 4
5 6 7 8 9
INHIBICIN ENZIMTICA
Los inhibidores enzimticos son aquellos agentes que interfieren con la catlisis,
disminuyendo o deteniendo la reaccin enzimtica. Se dividen en 2 grandes grupos:
1.- INHIBICIONES REVERSIBLES 2.- INHIBICION IREVERSIBLE
Inhibicin no competitiva
Inhibicin competitiva y
Inhibicin acompetitiva
INHIBICIN COMPETITIVA
El inhibidor generalmente tiene una estructura quimica semejante al sustrato, por lo tanto
puede combinarse con la enzima libre, de tal modo que compite con el sustrato especifico por
el sitio cataltico. Una caracterstica de este tipo de inhibicin est dada por el hecho de que
puede ser revertida aumentando la concentracin de sustrato.
Sustrato
Inhibidor
Competitivo
Inhibidor Competitivo
INHIBICIN NO COMPETITIVA
El inhibidor no tiene una estructura semejante a
la del sustrato, por lo tanto se une a un sitio
activo diferente al sitio catalitico de la enzima,
deformndola de tal manera que no puedan
formarse el complejo enzima-sustrato (ES).
No existe competencia por el sitio catalitico
entre el sustrato y el inhibidor.
Sustrato
Sustrato
Inhibidor
No Competitivo
Inhibidor No competitivo
INHIBICIN IRREVERSIBLE:
El inhibidor produce un cambio permanente en la molcula de enzima, que resulta en un
deterioro definitivo de su capacidad cataltica.
Por lo general estos inhibidores modifican qumicamente residuos de aminocidos en la
enzima que tienen funciones fundamentales en la catlisis.
INHIBICION ACOMPETITIVA
El inhibidor no tiene ninguna semejanza estructural con el sustrato, se une a un sitio activo
de la enzima, pero no se une a la enzima sola, este se une al complejo ES, formando de
esta manera un complejo ESI.
Sustrato
Inhibidor
Acompetitivo
Inhibidor Acompetitivo
REGULACION O MODULACION ENZIMATICA
Los reguladores alostricos actan como co-sustratos, se unen a la enzima en un lugar
especifico denominado sitio alostricos.
Efectores Positivos: se unen a la enzima, modificando el sitio cataltico para que se una
el sustrato y asi pueda este transformarse en productos.
Efectores Negativos: se unen a la enzima, modificando la estructura del sitio cataltico de
tal manera que ya no se pueda unir al sustrato, por lo tanto no se forma los productos.
REGULACION ALOSTERICA
Sitio
Alostrico
SUSTRATO
ENZIMA
Efector
Positivo
Sitio
Cataltico
PRODUCTOS
Sitio
Alostrico
ENZIMA
SUSTRATO
PRODUCTOS
Efector
Negativo
NO FORMACIN DE
PRODUCTOS
ENZIMA EFECTOR
NEGATIVO
ENZIMA EFECTOR
POSITIVO
Sitio
Cataltico
Se produce cuando la enzima que
regula el proceso sufre estados de
fosforilacion, este proceso es llevado a
cabo por enzimas denominadas
quinasas. Estas enzimas modifican su
actividad cataltica a travs de su unin
a un grupo qumico de pequeo
tamao (grupos fosfato). Estos grupos
sern eliminados posteriormente de la
enzima reguladora por enzimas
denominadas fosfatasas.
REGULACION COVALENTE
La enzima fosforilasa, se encuentra
en las celulas en un estado inactivo
de baja actividad llamada fosforilasa
b, la cual es convertida en
fosforilasa a activa, por adicin de
restos fosfato que se unen al
hidroxilo de residuos serina en la
molcula de la enzima.
FOSFORILASA
b (inactiva)
FOSFORILASA
a (activa)
QUINASA
FOSFATASA
FOSFORILASA a
(activa)
CADENA DE ALMIDON (n)
MOLECULA DE
GLUCOSA
GLUCOSA-1-FOSFATO CADENA DE ALMIDON (n-1)
REGULACION POR
RETROALIMENTACION
Este tipo de modulacin se caracteriza por que la
enzima clave en la ruta sinttica es inhibida por
los productos finales, lo que da como resultado la
interrupcin del proceso metablico.
Tambin se denomina regulacin por
retroinhibicin (inhibicin feed-back), es decir el
producto regula su propia sntesis.
VIA DE NOVO
VIA DE REUTILIZACION
CIDOS
NUCLEICOS
Вам также может понравиться
- Proyecto de TítuloДокумент77 страницProyecto de TítuloFabián HermosillaОценок пока нет
- ENZIMASДокумент31 страницаENZIMASpablo escobarОценок пока нет
- CNC LASer 2.0Документ43 страницыCNC LASer 2.0Nando Martinez Sandoval100% (1)
- Unidad 3 EnzimasДокумент42 страницыUnidad 3 EnzimasGar Ara100% (1)
- Edvard MunchДокумент5 страницEdvard MunchJaquelinaa AriasОценок пока нет
- Traduccion Aproximada Fases y Proceso de Marisa PeerДокумент51 страницаTraduccion Aproximada Fases y Proceso de Marisa Peerjoshua lancaster100% (1)
- Acceso a Universidad para Mayores de 25 años. Biología 2013-2017.: Solucionario Pruebas 2013-2017От EverandAcceso a Universidad para Mayores de 25 años. Biología 2013-2017.: Solucionario Pruebas 2013-2017Оценок пока нет
- ENZIMAS bIOQUÍMICAДокумент37 страницENZIMAS bIOQUÍMICANoelis LimonОценок пока нет
- Biocatalizadores y Referencias BibliograficasДокумент6 страницBiocatalizadores y Referencias BibliograficasMaria Elizabeth M. Alberca0% (1)
- Clorhidroxido de AluminioДокумент9 страницClorhidroxido de Aluminiosilvio latiniОценок пока нет
- ENZIMASДокумент38 страницENZIMASClaudia LoredoОценок пока нет
- Enzimas PDFДокумент20 страницEnzimas PDFEver VillanuevaОценок пока нет
- Tema 1 EnzimasДокумент25 страницTema 1 EnzimasCristhian Macalupú ArismendizОценок пока нет
- EnzimasДокумент29 страницEnzimasmanu92egОценок пока нет
- Enzimas Uss PDFДокумент34 страницыEnzimas Uss PDFClaudia Diaz ChuquilinОценок пока нет
- Enzimas UssДокумент37 страницEnzimas UssPilarОценок пока нет
- Enzymes in DDДокумент92 страницыEnzymes in DDDaniel Casas TelloОценок пока нет
- Concepto de Enzimas Capsula 1Документ4 страницыConcepto de Enzimas Capsula 1Ariel MojicaОценок пока нет
- EnzimasДокумент45 страницEnzimasraphaelОценок пока нет
- AminoacidosДокумент91 страницаAminoacidosLeidi BarreraОценок пока нет
- Taller EnzimasДокумент4 страницыTaller EnzimasRosman Ramos MartinezОценок пока нет
- BiologiaДокумент22 страницыBiologiaFercho MariscalОценок пока нет
- Trabajo Práctico de Biología NM #3 - Experimentos EnzimáticosДокумент16 страницTrabajo Práctico de Biología NM #3 - Experimentos EnzimáticosJeremy Palma80% (10)
- ENZIMAS BioquimicaДокумент34 страницыENZIMAS BioquimicadianaОценок пока нет
- Perfil de Lipidos 1Документ28 страницPerfil de Lipidos 1GonzaloОценок пока нет
- Enzimas y CofactoresДокумент74 страницыEnzimas y CofactoresJeimykОценок пока нет
- ENZIMASДокумент21 страницаENZIMASjaelОценок пока нет
- Bonilla-Juardo-Saavedra-Tabares-Ortiz - Taller Enzimas AДокумент10 страницBonilla-Juardo-Saavedra-Tabares-Ortiz - Taller Enzimas ANicol andrea Saavedra orozcoОценок пока нет
- En ZimasДокумент15 страницEn ZimasCarlos CanchisОценок пока нет
- 3 EnzimasДокумент63 страницы3 EnzimasKamila MartinezОценок пока нет
- En ZimasДокумент44 страницыEn ZimasMIRIAM SARAI BETANCOURT CABRERAОценок пока нет
- Enzimas BioquimicaДокумент54 страницыEnzimas BioquimicaElvia MezaОценок пока нет
- EnzimasДокумент50 страницEnzimasGato QuequeОценок пока нет
- Sesión 01 - Generalidades de Las EnzimasДокумент16 страницSesión 01 - Generalidades de Las EnzimasaravelloriОценок пока нет
- Informe BioquimicДокумент12 страницInforme BioquimicDarwin AmasifuenОценок пока нет
- Investigacion #6 Funcion y Clasificacion de EnzimasДокумент6 страницInvestigacion #6 Funcion y Clasificacion de EnzimasJessica LaraОценок пока нет
- ENZIMIOLOGÍA - Obstetricia PDFДокумент65 страницENZIMIOLOGÍA - Obstetricia PDFDerecho IcaОценок пока нет
- BIOLOGIAДокумент12 страницBIOLOGIAYanixa Vivar MauricioОценок пока нет
- Enzimas Cap. 6 Ferrier.Документ8 страницEnzimas Cap. 6 Ferrier.Evelyn Guadalupe González BravoОценок пока нет
- ENZIMASДокумент19 страницENZIMASneiver flores100% (1)
- Los Enzimas Son Proteínas Que Catalizan Reacciones Químicas en Los Seres VivosДокумент5 страницLos Enzimas Son Proteínas Que Catalizan Reacciones Químicas en Los Seres VivosJahana GarciaОценок пока нет
- 2 Enzimas 2016Документ7 страниц2 Enzimas 2016Estela EscalanteОценок пока нет
- Informe EnzimaticoДокумент4 страницыInforme Enzimaticojose franciscoОценок пока нет
- Bbioquimica de Los Alimentos Enzimas en Panaderia y ConfiteriaДокумент37 страницBbioquimica de Los Alimentos Enzimas en Panaderia y ConfiteriaJerson David Rubín TorresОценок пока нет
- Enzimas e Introduccion Al MetabolsimoДокумент27 страницEnzimas e Introduccion Al MetabolsimoTino JFОценок пока нет
- CAP 4. EnzimasДокумент52 страницыCAP 4. EnzimasCarlos Paul TitoОценок пока нет
- 13 EnzimasДокумент55 страниц13 EnzimasricardoОценок пока нет
- Enzimologia Clínica 2022Документ75 страницEnzimologia Clínica 2022Fanny ChavezОценок пока нет
- Bioquimica Tercer ParcialДокумент39 страницBioquimica Tercer Parcialsabriii Mapofseul7 BTSОценок пока нет
- Cinética Enzimática, ReporteДокумент6 страницCinética Enzimática, ReporteHeriberto Angeles0% (3)
- Diapo Semana 9Документ29 страницDiapo Semana 9Eddisom PathinОценок пока нет
- EnzimasДокумент9 страницEnzimasVinicio BermudezОценок пока нет
- Enzimas PDFДокумент53 страницыEnzimas PDFNelson BeltranОценок пока нет
- ENZIMASДокумент22 страницыENZIMASJosselin Jazmin Zanga QuispeОценок пока нет
- Cinetica EnzimaticaДокумент7 страницCinetica EnzimaticaAndreaBenitezОценок пока нет
- En ZimasДокумент58 страницEn ZimasRubela María Rojas PumaОценок пока нет
- 08 EnzimasДокумент44 страницы08 EnzimasCarlos M. Guerra AОценок пока нет
- Enzimas BioquimicaДокумент45 страницEnzimas BioquimicaJcaminoОценок пока нет
- Semana 11 Enzimas UssДокумент64 страницыSemana 11 Enzimas UssKarely CFОценок пока нет
- Semana 01 EnzimasДокумент14 страницSemana 01 EnzimasFatima Palacios GeronimoОценок пока нет
- EnzimasДокумент21 страницаEnzimasLuisa BernalОценок пока нет
- Discusión Nº 3 de EnzimasДокумент7 страницDiscusión Nº 3 de EnzimasRené Belisario Carranza56% (9)
- Metabolismo CelularДокумент9 страницMetabolismo CelularamandaОценок пока нет
- Enzimas A BДокумент41 страницаEnzimas A BJlAОценок пока нет
- Nuevo Documento de Microsoft WordДокумент1 страницаNuevo Documento de Microsoft WordMiguel AngelОценок пока нет
- C.V GuevaraДокумент3 страницыC.V GuevaraMiguel AngelОценок пока нет
- CARATULA UpaoДокумент1 страницаCARATULA UpaoMiguel AngelОценок пока нет
- Antracnosis en PaltoДокумент66 страницAntracnosis en PaltoMiguel Angel100% (1)
- Cultivo de CamoteДокумент18 страницCultivo de CamoteMiguel AngelОценок пока нет
- Trabajo UpaoДокумент2 страницыTrabajo UpaoMiguel AngelОценок пока нет
- Cultivo de PiñaДокумент6 страницCultivo de PiñaMiguel AngelОценок пока нет
- Biosintesis Del Grupo HemoДокумент8 страницBiosintesis Del Grupo HemoMiguel AngelОценок пока нет
- Quimico de HecesДокумент19 страницQuimico de HecesJesús Adrián Gómez OrtizОценок пока нет
- 2.2 Planilla de Mayores Metrados - MarzoДокумент157 страниц2.2 Planilla de Mayores Metrados - MarzoJHON ANDER VELASQUEZ CUELLARОценок пока нет
- Informe Preliminar Contratos Con Altos Montos Contratados y Tramites ExternosДокумент33 страницыInforme Preliminar Contratos Con Altos Montos Contratados y Tramites ExternosKatherine MartinezОценок пока нет
- Juana Castro, María Zambrano, MadridДокумент7 страницJuana Castro, María Zambrano, MadridRÓBINSON ANTONIO CASTRO PEINADOОценок пока нет
- Grupo 03, Tarea 03Документ35 страницGrupo 03, Tarea 03JOSE LUIS HUAMAN CHAVEZОценок пока нет
- 01 Problemas de Genética I. Las Leyes de MendelДокумент2 страницы01 Problemas de Genética I. Las Leyes de MendelalmudenaОценок пока нет
- Bloqueo de TobilloДокумент28 страницBloqueo de TobilloKarla De León Vega100% (1)
- ESPONDAДокумент4 страницыESPONDAJoseAngelPalaciosCamposОценок пока нет
- Balanza de PagosДокумент4 страницыBalanza de Pagosnatalia ballinaОценок пока нет
- PresbifoniaДокумент25 страницPresbifoniaCamila Paz100% (2)
- Taller #1 Seguimiento #1 Cal Vectorial I 2021 UPBДокумент1 страницаTaller #1 Seguimiento #1 Cal Vectorial I 2021 UPBcaft trujilloОценок пока нет
- Guia de Ejercicios FASTTOOL EJ1 EJ2 EJ3 EJ4Документ49 страницGuia de Ejercicios FASTTOOL EJ1 EJ2 EJ3 EJ4eduardo contrerasОценок пока нет
- El Hundimiento Del Vapor Maldonado, Diario El Pueblo de Santa LuciaДокумент28 страницEl Hundimiento Del Vapor Maldonado, Diario El Pueblo de Santa Luciafponto9928100% (1)
- Inspección Y Prueba de IndicadoresДокумент2 страницыInspección Y Prueba de IndicadoresAlisson Nallely Matallanes CastilloОценок пока нет
- L8 - Motor Sincrono Trifasico (NEW) JCДокумент20 страницL8 - Motor Sincrono Trifasico (NEW) JCbertha100% (1)
- Clasificación de Los Volcanes y Sus CaracterísticasДокумент3 страницыClasificación de Los Volcanes y Sus CaracterísticasNohemy Garzón100% (1)
- San Pedro Mártir de VeronaДокумент18 страницSan Pedro Mártir de VeronaHugoRodriguezSanMiguelОценок пока нет
- MODI-Sem1-Teoría Del RiesgoДокумент86 страницMODI-Sem1-Teoría Del RiesgoRayme RòmuloОценок пока нет
- Procesos AuxiliaresДокумент30 страницProcesos AuxiliaresJosé Manuel M.L.Оценок пока нет
- Informe de HelicesДокумент3 страницыInforme de HelicesyessОценок пока нет
- Sapognikoff TP4 V1Документ3 страницыSapognikoff TP4 V1Guido SapognikoffОценок пока нет
- Ribes (2016) - La Psicologia. Que InvestigarДокумент12 страницRibes (2016) - La Psicologia. Que InvestigarMine RHОценок пока нет
- Pasaje LATAMДокумент2 страницыPasaje LATAMJhesus GarciaОценок пока нет
- Experiencias en El Uso de La Herramienta TRENDSДокумент17 страницExperiencias en El Uso de La Herramienta TRENDSGrupo Scout Ocho MocaОценок пока нет
- Didáctica de La Matemática TP 3Документ12 страницDidáctica de La Matemática TP 3NOELIA SOLEDAD SANCHEZОценок пока нет