Академический Документы
Профессиональный Документы
Культура Документы
Kimfis Allohu Akbar
Загружено:
Nafilatul Arfa0 оценок0% нашли этот документ полезным (0 голосов)
2 просмотров6 страницkimia fisika
Авторское право
© © All Rights Reserved
Доступные форматы
PPTX, PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документkimia fisika
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате PPTX, PDF, TXT или читайте онлайн в Scribd
0 оценок0% нашли этот документ полезным (0 голосов)
2 просмотров6 страницKimfis Allohu Akbar
Загружено:
Nafilatul Arfakimia fisika
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате PPTX, PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 6
Temperatur dan Tekanan Konstan
Pada tekanan dan suhu konstan, maka dT dan dP
dinyatakan nol. Sehingga,
dG = -Sdt + Vdp +dn
dG = 0 + AdnA + BdnB
Menggunakan prosedur yang sama pada contoh volume
konstan, maka
dG = dnB[o + RT ln pB 2RT ln pA ]
pA = tekanan parsial NO2 dan pB = tekanan parsial N2O4
Walaupun kita menggunakan prosedur volume konstan,
namun pada bagian ini volume gas adalah tidak konstan.
Karena volume tidak konstan,maka berlaku
PV = nRT
+ 2+
V= = = =
Dengan mensubstitusikan persamaan diatas
maka,
dG = dnB [o + RT ln(ponB) 2RT ln(po(no-
2nB))]+ RT ln(no-nB)
Untuk mendapatkan energi bebas, maka harus
dengan mengintegralkan persamaan diatas.
Sehingga diperoleh,
G = noAo+ nBo + RT[nBln(ponB) + (no
2nB)ln(po(no -2nB)) + (nB-no)ln(no-nB)]
Gambar 3
Gambar 4
Вам также может понравиться
- Up 17 Suhu Dan KalorДокумент66 страницUp 17 Suhu Dan KalorNafilatul ArfaОценок пока нет
- Kisi Sas B.indo Ganjil 2324Документ4 страницыKisi Sas B.indo Ganjil 2324Nafilatul ArfaОценок пока нет
- Kisi-Kisi Alquran Hadits PAS Gasal FixДокумент6 страницKisi-Kisi Alquran Hadits PAS Gasal FixNafilatul ArfaОценок пока нет
- Kisi Kisi Sas Gasal B. Arab KLS 7 2023 2024Документ12 страницKisi Kisi Sas Gasal B. Arab KLS 7 2023 2024Nafilatul ArfaОценок пока нет
- Kisi Kisi PAS 9 2021Документ5 страницKisi Kisi PAS 9 2021Nafilatul ArfaОценок пока нет
- Kisi-Kisi PAS Ganjil IPA VIIIДокумент6 страницKisi-Kisi PAS Ganjil IPA VIIINafilatul ArfaОценок пока нет
- Kisi Kisi Ujian Praktek Fikih Dan Pedoman PenskoranДокумент2 страницыKisi Kisi Ujian Praktek Fikih Dan Pedoman PenskoranNafilatul ArfaОценок пока нет
- Lampiran Kekentalan FluidaДокумент2 страницыLampiran Kekentalan FluidaNafilatul ArfaОценок пока нет
- Usaha Energi FisdasДокумент19 страницUsaha Energi FisdasIsni NuraniОценок пока нет
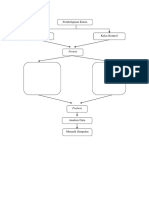
- Alur PenelitianДокумент1 страницаAlur PenelitianNafilatul ArfaОценок пока нет
- Rpppramukapenggalang 140917231801 Phpapp01Документ26 страницRpppramukapenggalang 140917231801 Phpapp01BaehakiОценок пока нет
- Bahan Ajar Termokimia KD 3.4Документ7 страницBahan Ajar Termokimia KD 3.4Nafilatul ArfaОценок пока нет
- Kerangka BerpikirДокумент2 страницыKerangka BerpikirNafilatul ArfaОценок пока нет
- Prinsip Manajemen KurikulumДокумент28 страницPrinsip Manajemen KurikulumNafilatul ArfaОценок пока нет
- Fungsi Manajemen KurikulumДокумент43 страницыFungsi Manajemen KurikulumNafilatul ArfaОценок пока нет
- Kalori MeterДокумент2 страницыKalori MeterNafilatul ArfaОценок пока нет
- KalorimeterДокумент3 страницыKalorimeterFajar RumantoОценок пока нет
- ResonansiДокумент10 страницResonansiNafilatul Arfa0% (1)
- Kalori MeterДокумент2 страницыKalori MeterNafilatul ArfaОценок пока нет
- Presentasi PancasilaДокумент14 страницPresentasi PancasilaNafilatul ArfaОценок пока нет
- TorricelliДокумент7 страницTorricelliNafilatul ArfaОценок пока нет
- KalorimeterДокумент8 страницKalorimeterNafilatul ArfaОценок пока нет
- Kebudayaan PancasilaДокумент12 страницKebudayaan PancasilaNafilatul ArfaОценок пока нет
- Kebudayaan PancasilaДокумент12 страницKebudayaan PancasilaNafilatul ArfaОценок пока нет
- PKN PORNOGRAFIДокумент8 страницPKN PORNOGRAFINafilatul ArfaОценок пока нет
- Presentasi PancasilaДокумент14 страницPresentasi PancasilaNafilatul ArfaОценок пока нет
- Panca SilaДокумент7 страницPanca SilaNafilatul ArfaОценок пока нет
- Arti MTKДокумент8 страницArti MTKNafilatul ArfaОценок пока нет
- Aplikasi Diferensial Dalam KimiaДокумент15 страницAplikasi Diferensial Dalam KimiaNafilatul ArfaОценок пока нет
- Ekosistem Klmpok 5Документ24 страницыEkosistem Klmpok 5Isni NuraniОценок пока нет