Академический Документы
Профессиональный Документы
Культура Документы
Alquenos
Загружено:
Chris Flores Gonzales0 оценок0% нашли этот документ полезным (0 голосов)
114 просмотров18 страницEste documento describe las propiedades físicas y químicas de los alquenos. Los primeros tres alquenos son gases, los siguientes 11 son líquidos, y los restantes son sólidos. Las propiedades como punto de ebullición y fusión aumentan con el peso molecular. Químicamente son reactivos y pueden sufrir reacciones de combustión, adición y polimerización. El etileno es el alqueno más importante y se usa ampliamente en la industria para producir muchos compuestos.
Исходное описание:
Оригинальное название
alquenos.ppt
Авторское право
© © All Rights Reserved
Доступные форматы
PPT, PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документEste documento describe las propiedades físicas y químicas de los alquenos. Los primeros tres alquenos son gases, los siguientes 11 son líquidos, y los restantes son sólidos. Las propiedades como punto de ebullición y fusión aumentan con el peso molecular. Químicamente son reactivos y pueden sufrir reacciones de combustión, adición y polimerización. El etileno es el alqueno más importante y se usa ampliamente en la industria para producir muchos compuestos.
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате PPT, PDF, TXT или читайте онлайн в Scribd
0 оценок0% нашли этот документ полезным (0 голосов)
114 просмотров18 страницAlquenos
Загружено:
Chris Flores GonzalesEste documento describe las propiedades físicas y químicas de los alquenos. Los primeros tres alquenos son gases, los siguientes 11 son líquidos, y los restantes son sólidos. Las propiedades como punto de ebullición y fusión aumentan con el peso molecular. Químicamente son reactivos y pueden sufrir reacciones de combustión, adición y polimerización. El etileno es el alqueno más importante y se usa ampliamente en la industria para producir muchos compuestos.
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате PPT, PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 18
PROPIEDADES FÍSICAS
A la temperatura y presión ordinarias los
tres primeros alquenos normales son
gases (C2H4 al C4H8); los once siguientes
son líquidos (C5H10 al C15H30); y los
términos superiores son sólidos, fusibles
y volátiles sin descomposición, a partir
del C16H32.
Por lo general, el punto de ebullición, el de
fusión, la viscosidad y la densidad
aumentan conforme el peso molecular.
Nombres Punto de
Fórmula Punto de Densidad (a
ebullición
Oficial Común Molecular fusión (°C) 20°C)
(°C)
Eteno Etileno C2H4 -169.4° -102.4° ----
Propeno Propileno C3H6 -185° -47.7 ----
1Buteno o-butileno C4H8 -185.8° -6.5 .0617
1Penteno o-amileno C5H10 -166° 30.1 .643
1Hexeno o-hexileno C6H12 -138° 63.5 .675
1Hepteno o-heptileno C7H14 -119.1° 93.1 .698
1Octeno o-octileno C8H16 -104° 122.5 .716
Los alquenos son incoloros, muy
ligeramente solubles en agua y sin olor,
pero el etileno tiene un suave olor
agradable.
PROPIEDADES QUÍMICAS
Los alquenos presentan una gran
reactividad química debido a que un
doble enlace es más débil que un enlace
simple.
Las reacciones características de estos
compuestos son la combustión, la
reacción de adición y la polimerización.
Reacción de combustión
Los alquenos como todos los compuestos
orgánicos son combustibles. Arden con llama
más luminosa que los alcanos originando
combustiones completas e incompletas.
Combustión completa del eteno
C2H 4 (g) +3O2 (g) 2CO2(g) + 2H2O (g) + energía
Eteno Dióxido de agua
Carbono
Reacción de Adición:
En éstas reacciones se rompe el doble enlace del
alqueno y se incorpora a él la molécula de
hidrógeno o los halógenos. Puede originarse un
alcano o un derivado alcano.
CH2=CH2(g)+H2(g) CH3- CH3(g)
eteno etano
CH2=CH-CH3(g)+Br2 (l) CH2 Br -CH Br -CH3(g)
propeno 1,3-dibromopropano
Reacción de Polimerización. Los alquenos
pueden polimerizarse fácilmente, para ello al
calentarlos y en presencia de catalizadores se
rompe el doble enlace formando unas especies
químicas inestables. Estas especies químicas se
unen entre sí, formando largas cadenas que son
los polímeros.
CH2=CH2(g)+H2(g) (-CH2-CH2 -)nS
Eteno polieteno
PREPARACIÓN DE LOS ALQUENOS
Se conocen numerosos métodos para obtener
alcanos, pero por su sencillez e importancia,
consideramos fundamentales:
Erlenmeyer.- Consiste en deshidratar los derivados
monohidroxilados de hidrocarburos saturados a la
temperatura de 170°C por el ácido sulfúrico; pero la
deshidratación también puede realizarse por el
H3PO4, el P2O5, el Al2O3, el KHSO4, los ácidos oxálicos
y fórmico, en condiciones apropiadas.
Cuando se emplea como deshidratante el H2SO4,
la reacción se verifica en dos fases. En la primera
fase se forma sulfato ácido de alquilo (ácido
sulfovínico), el cual, a la temperatura elevada de
la reacción se descompone, regenerando el ácido
sulfúrico y produciendo el alqueno:
1ra fase
CH3-CH2-OH + HOSO2.OH ------------> H20 + CH3-CH2-O.SO2OH
2da fase
CH3-CH2-O.SO2.OH --(170°C)--> H2SO4 + CH2=CH2
Cracking.- Hidrocarburos superiores son
sometidos a temperaturas y presiones
convenientes.
CH3-(CH2)4-CH3 ---(Calor y presión)--- CH3-(CH2)2-CH3 + CH2=CH2
APLICACIONES GENERALES DE ALQUENOS
Eteno o etileno.- También llamado gas
oleificante. Descubierto en 1795 por los
químicos holandeses Deiman, Paetz Van
Troostwyk, Bond y Lauwrenburgh,
deshidratando el alcohol etílico por el ácido
sulfúrico.
Se le ha llamado gas oleificante porque con
el cloro produce cloruro de etileno (dicloro
1,2-etano) que es una sustancia de
consistencia aceitosa.
Es un gas incoloro de suave olor agradable,
que puede prepararse por los métodos
generales ya expuestos; pero, en el
laboratorio se prefiera deshidratar el
alcohol etílico mediante el ácido sulfúrico.
El etileno es muy empleado en la
industria. Se le considera como la más
importante materia prima para la
producción de compuestos
alifáticos. Solamente en los Estados Unidos
de Norteamérica se producen anulmente
más de 250 millones de litros de etanol y
más de 1,000 millones de ligros de
etilenglicol a partir del etileno.
Se emplea como anestésico en Cirugía, y
en gran escala para la maduración de
frutas, como limones, manzanas, toronjas,
naranjas, plátanos, etc.
El etileno exhibe propiedades semejantes a
las hormonas acelerando el crecimiento de
varios tubérculos, como la patata.
Grandes cantidades de etileno se consumen en
la preparación de dicloruro de etileno, el cual se
emplea como solvente en la manufactura de
insecticidas, así como en la producción del tikol
que es un sustituto del hule, y del etilenglicol
usado en la producción del dulux.
Condensando el etileno y la acetona se produce el
isopreno, base del hule artificial o sintético.
El etileno presenta poca tendencia a la
polimerización; sin embargo, en condiciones
especiales (1 000 atmósferas y presencia de trazas
de oxígeno) se consigue su polimerización.
El producto sintético polietileno, es
extraordinariamente resistente a las acciones
químicas, y está constituido por centenares de
moléculas de etileno.
Con el benceno, el etileno produce el
etilbenceno, que por deshidrogenación a elveada
temperatura (700°C) y de oxido de aluminio da el
estireno, que constituye el monómero del
Poliestireno y del Buna S.
El Buna S es el ejemplo de polimerización mixta,
la cual se logra con sodio, aunque actualmente se
realiza en emulsión acuosa mediante peroxidos.
Вам также может понравиться
- Gravimetría Por VolatilizaciónДокумент2 страницыGravimetría Por VolatilizaciónDDanii MoraLes RanGeel100% (2)
- Pardeamiento No Enzimatico en Leche Fresca Gloria y de VacaДокумент8 страницPardeamiento No Enzimatico en Leche Fresca Gloria y de VacaLizeth HerediaОценок пока нет
- COMPOSICIÓN PORCENTUAL MASA VolumenДокумент5 страницCOMPOSICIÓN PORCENTUAL MASA VolumenLuis Enrique Quispe HanccoОценок пока нет
- Práctica #6Документ9 страницPráctica #6Nelson Estela ValenzuelaОценок пока нет
- ExtracciónДокумент4 страницыExtracciónGerardo Avendaño TrianaОценок пока нет
- Practica 8. PRINCIPIO DE LA CONSERVACIÓN DE LA MATERIA-1Документ4 страницыPractica 8. PRINCIPIO DE LA CONSERVACIÓN DE LA MATERIA-1lyfaОценок пока нет
- Biorreactores para El Cultivo de Células de Animales y PlantasДокумент37 страницBiorreactores para El Cultivo de Células de Animales y PlantasRicardoОценок пока нет
- Taller 3-2 Aldehídos y CetonasДокумент4 страницыTaller 3-2 Aldehídos y CetonasJavier ContrerasОценок пока нет
- Guia N°5 Geoemetria MolecularДокумент2 страницыGuia N°5 Geoemetria MolecularDamy Clavijo Sepulveda100% (1)
- Practica Laboratorio Ii A1Документ10 страницPractica Laboratorio Ii A1Itzel López EugenioОценок пока нет
- Indicadores de PH CaserosДокумент15 страницIndicadores de PH CaserosMech RugalОценок пока нет
- DESTILACIÓNДокумент3 страницыDESTILACIÓNPipizlOve MijaresОценок пока нет
- Práctica. Extracción Sólido LíquidoДокумент6 страницPráctica. Extracción Sólido LíquidoSarai Arce ArellanoОценок пока нет
- Practica PH en AlimentosДокумент13 страницPractica PH en AlimentosCarolina Hernández MontañoОценок пока нет
- Proyecto FinalДокумент25 страницProyecto FinallplualuchaОценок пока нет
- Cinetica Quimica Unidad IIIДокумент15 страницCinetica Quimica Unidad IIIAngel Irahola EstradaОценок пока нет
- Taller 4Документ6 страницTaller 4Sebastian CandoОценок пока нет
- Obtencion Cloruro de SodioДокумент3 страницыObtencion Cloruro de Sodiolisseth calleОценок пока нет
- El Ciclo de CalvinДокумент4 страницыEl Ciclo de Calvingrissel hernandezОценок пока нет
- Practica Uso de La Remolacha Como Indicador de PHДокумент1 страницаPractica Uso de La Remolacha Como Indicador de PHVanessa González50% (2)
- CicloAlcanos-Cicloalquenos y CicloalquinosДокумент2 страницыCicloAlcanos-Cicloalquenos y CicloalquinosMaría MonasterioОценок пока нет
- Isomeria 2Документ24 страницыIsomeria 2Joseph EstradaОценок пока нет
- Práctica 4 CristalizaciónДокумент9 страницPráctica 4 CristalizaciónOmar JuarezОценок пока нет
- Problema de Evaporadores 2019Документ4 страницыProblema de Evaporadores 2019Briseida Jacinto ChamochumbiОценок пока нет
- Marco TeoricoДокумент4 страницыMarco TeoricoAna Luz MoyaОценок пока нет
- Examen Parcial de Procesos INDUSTRIALES 2016-2Документ3 страницыExamen Parcial de Procesos INDUSTRIALES 2016-2sergio0% (1)
- Tipos de SolucionДокумент6 страницTipos de SolucionYimi Peralta VegaОценок пока нет
- Cambiadores de Calor de Camisa y SerpentínДокумент15 страницCambiadores de Calor de Camisa y Serpentínmonica jimenezОценок пока нет
- Modelo Focus GroupДокумент3 страницыModelo Focus GroupDiana FloresОценок пока нет
- Diapositivas Fisicoquimica - TensoactivosДокумент17 страницDiapositivas Fisicoquimica - Tensoactivosmaicolahumedom84Оценок пока нет
- Reacciones de AlcanosДокумент8 страницReacciones de AlcanosArturo GarciaОценок пока нет
- Modelo Matematico de Torre de DestilacionДокумент16 страницModelo Matematico de Torre de DestilacionMarinely OviedoОценок пока нет
- ButanonaДокумент5 страницButanonaJoseph ZamoraОценок пока нет
- Cuestionario 1.1 Seleccionar Material de LaboratorioДокумент25 страницCuestionario 1.1 Seleccionar Material de LaboratorioGERALDINE GONZALEZ POLANCOОценок пока нет
- Tablas 001Документ42 страницыTablas 001Jose Ignacio Manriquez AvendañoОценок пока нет
- Práctica (M.R.U-M.R.U.V)Документ6 страницPráctica (M.R.U-M.R.U.V)Natalia QuirogaОценок пока нет
- Teoria 8 - Examen de Primera UnidadДокумент3 страницыTeoria 8 - Examen de Primera UnidadMaria AquinoОценок пока нет
- Guia de Ejercicios 4 Segunda Ley de La Termodinamica y EntropiaДокумент5 страницGuia de Ejercicios 4 Segunda Ley de La Termodinamica y EntropiaFrancis ValerioОценок пока нет
- 4.2 TermoquimicaДокумент31 страница4.2 Termoquimicaleonardo3744Оценок пока нет
- NomenclaturaДокумент8 страницNomenclaturaR JandikОценок пока нет
- TPNº5 Cinética Química 2018Документ3 страницыTPNº5 Cinética Química 2018Leonardo GimenezОценок пока нет
- Informe. Práctica 3Документ11 страницInforme. Práctica 3Melina HernándezОценок пока нет
- Manual de Laborartorio de Química IIДокумент58 страницManual de Laborartorio de Química IIJavier AguilarteОценок пока нет
- ALCOHOLESДокумент4 страницыALCOHOLESValeria Espinel VeraОценок пока нет
- Tipos de Reacciones Según Las Fases de Los ReaccionantesДокумент15 страницTipos de Reacciones Según Las Fases de Los ReaccionantesEnder J. Maldonado100% (1)
- Práctica N°05 - Cinetica de SecadoДокумент3 страницыPráctica N°05 - Cinetica de SecadodelbhergarciamedinaОценок пока нет
- U1 - S1 - Ficha de Trabajo 1-Estructura Del Átomo, Tabla Periódica y Enlaces InteratómicosДокумент3 страницыU1 - S1 - Ficha de Trabajo 1-Estructura Del Átomo, Tabla Periódica y Enlaces InteratómicosMaycillo MiranОценок пока нет
- Quimica Cap 10Документ65 страницQuimica Cap 10Mark CastilloОценок пока нет
- Mezclas BinariasДокумент9 страницMezclas BinariasLyseth Karina Gómez RoseroОценок пока нет
- Informe Calorimetria 3Документ15 страницInforme Calorimetria 3vaudevilleeОценок пока нет
- Inquimica 1Документ5 страницInquimica 1JonathanAndrésОценок пока нет
- Trabajo PracticoДокумент11 страницTrabajo PracticoCaro JuradoОценок пока нет
- Informe de AlcanosДокумент17 страницInforme de AlcanosTania Limachi Diaz100% (1)
- ETILENOДокумент13 страницETILENOWilliam Ledesma MascaroОценок пока нет
- Expo Olefinas 120606212042 Phpapp02Документ44 страницыExpo Olefinas 120606212042 Phpapp02Danny Lugo100% (1)
- 9 - Quimica-Alcoholes-Kinesio-10Документ54 страницы9 - Quimica-Alcoholes-Kinesio-10Gustavo TulaОценок пока нет
- Resumen de Los AlquenosДокумент2 страницыResumen de Los AlquenossteelcraftОценок пока нет
- Sintesis y Propiedades Quimicas de Los AlquenosДокумент15 страницSintesis y Propiedades Quimicas de Los AlquenosJuan Carlos Escalera Vallejos50% (2)
- ALQUENOSДокумент6 страницALQUENOSEnrique Rojas BermudoОценок пока нет
- Lectura Dignidad de La ProfesiònДокумент6 страницLectura Dignidad de La ProfesiònChris Flores GonzalesОценок пока нет
- Silabo de Genetica)Документ9 страницSilabo de Genetica)Marco MinayaОценок пока нет
- Comunicado Examen Final de Casos Integradores IiДокумент1 страницаComunicado Examen Final de Casos Integradores IiChris Flores GonzalesОценок пока нет
- LecturaДокумент3 страницыLecturaChris Flores GonzalesОценок пока нет
- Caso DiabetesДокумент2 страницыCaso DiabetesChris Flores GonzalesОценок пока нет
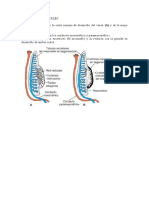
- Conductos GenitalesДокумент1 страницаConductos GenitalesChris Flores GonzalesОценок пока нет
- Booleanos MbeДокумент1 страницаBooleanos MbeChris Flores GonzalesОценок пока нет
- Receptores SomatosensorialesДокумент1 страницаReceptores SomatosensorialesChris Flores GonzalesОценок пока нет
- Comentario Sobre MedlineДокумент3 страницыComentario Sobre MedlineChris Flores GonzalesОценок пока нет
- 37 Megacolon Congenito PDFДокумент12 страниц37 Megacolon Congenito PDFIvon AlexandraОценок пока нет
- Silabo PDFДокумент11 страницSilabo PDFChris Flores GonzalesОценок пока нет
- CAP-I Biologia PreДокумент8 страницCAP-I Biologia PreRuth CornejoОценок пока нет
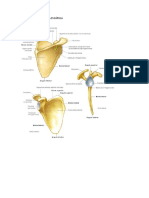
- Accidentes EscapulaДокумент1 страницаAccidentes EscapulaChris Flores GonzalesОценок пока нет
- Anatomia EscapulaДокумент1 страницаAnatomia EscapulaChris Flores GonzalesОценок пока нет
- Anatomia Del FemurДокумент1 страницаAnatomia Del FemurChris Flores GonzalesОценок пока нет
- Parti PoliticosДокумент1 страницаParti PoliticosChris Flores GonzalesОценок пока нет
- FenotipoДокумент1 страницаFenotipommmmm12Оценок пока нет
- Metodo CientificoДокумент3 страницыMetodo CientificoChris Flores GonzalesОценок пока нет
- Anatomía Del FemurДокумент1 страницаAnatomía Del FemurChris Flores GonzalesОценок пока нет
- La Elipse ExposicionДокумент18 страницLa Elipse ExposicionChris Flores Gonzales50% (2)
- FenotipoДокумент1 страницаFenotipommmmm12Оценок пока нет
- Parti PoliticosДокумент1 страницаParti PoliticosChris Flores GonzalesОценок пока нет
- Imperio IncaicoДокумент10 страницImperio IncaicoChris Flores GonzalesОценок пока нет
- Biografía de Ramón CastillaДокумент10 страницBiografía de Ramón CastillaChris Flores GonzalesОценок пока нет
- Estilos de AprendizajeДокумент31 страницаEstilos de AprendizajeChris Flores Gonzales100% (1)
- DogmaДокумент4 страницыDogmaChris Flores GonzalesОценок пока нет
- Tabla - Periodica Color 1 PDFДокумент2 страницыTabla - Periodica Color 1 PDFlauranoecepedaОценок пока нет
- Interactions Between Impression Materials and Immediate Dentin Sealing - En.esДокумент8 страницInteractions Between Impression Materials and Immediate Dentin Sealing - En.esBest MomentsОценок пока нет
- Addinol Gear Oil CLP 320 - E-EsДокумент8 страницAddinol Gear Oil CLP 320 - E-EsdanililloОценок пока нет
- Mercurio - Gas NaturalДокумент5 страницMercurio - Gas NaturalNicolasArgañarazОценок пока нет
- 11 Muro AgrietadoДокумент6 страниц11 Muro AgrietadoJorge Luis Olivos FajardoОценок пока нет
- CIRSOC 201 (2005) Reglamento PDFДокумент629 страницCIRSOC 201 (2005) Reglamento PDFingluceroОценок пока нет
- Sistema Contra Incendio de Una Planta (Caso Real)Документ25 страницSistema Contra Incendio de Una Planta (Caso Real)patricia isabel palma corderoОценок пока нет
- Metalurgia - Merrill CroweДокумент54 страницыMetalurgia - Merrill CroweFrank PachecoОценок пока нет
- Estructuras BifasicasДокумент8 страницEstructuras BifasicasArmando ChambiОценок пока нет
- Sintesis Del Mono Cloroacetico TextoДокумент4 страницыSintesis Del Mono Cloroacetico TextoWilly Alexander López AlvaОценок пока нет
- FISICOДокумент5 страницFISICOMaria RomeroОценок пока нет
- Especificaciones Tecnicas: Examen de Los Planos, Especificaciones Y Lugar de La ObraДокумент55 страницEspecificaciones Tecnicas: Examen de Los Planos, Especificaciones Y Lugar de La ObraIvonne Del PozoОценок пока нет
- Cemento PresentacionДокумент48 страницCemento Presentacionceleste salazar aguirreОценок пока нет
- Estándares CAD Ver AДокумент14 страницEstándares CAD Ver ABuenaventura TuestaОценок пока нет
- Computos MetricosДокумент1 страницаComputos MetricosGari SilesОценок пока нет
- Normalización de Los Materiales - Grupo 7Документ13 страницNormalización de Los Materiales - Grupo 7Eduar Ramirez SolsolОценок пока нет
- Modelació..3ra ParteДокумент143 страницыModelació..3ra ParteAntonio YamОценок пока нет
- Síntesis de Superplastificantes Base Policarboxilatos de Alto Desempeño para Concreto y MorteroДокумент12 страницSíntesis de Superplastificantes Base Policarboxilatos de Alto Desempeño para Concreto y MorteroKjielОценок пока нет
- Ejercicios AnionesДокумент2 страницыEjercicios AnionesDiego ZumaránОценок пока нет
- Vigueta Bovedilla Muy BuenoДокумент6 страницVigueta Bovedilla Muy BuenoEzequielPachecoMartinezОценок пока нет
- S5 - Clase 05 Sep HILATURA DE FIBRA CORTA eДокумент24 страницыS5 - Clase 05 Sep HILATURA DE FIBRA CORTA ePatrick P Rodriguez Gr100% (1)
- Costos Unitarios y Presupuestos Inst Sanitarias CHACoNДокумент28 страницCostos Unitarios y Presupuestos Inst Sanitarias CHACoNAlexОценок пока нет
- 10P007 Es MAXXIMA COFREEДокумент2 страницы10P007 Es MAXXIMA COFREEoctavio3EDОценок пока нет
- Tap 1180 2Документ2 страницыTap 1180 2Rubén D. Mamani Y.Оценок пока нет
- PQR Smaw E7018-6010Документ2 страницыPQR Smaw E7018-6010poulmackОценок пока нет
- P BiodieselДокумент15 страницP BiodieselAlejandro RamosОценок пока нет
- Vidrios y AsbestoДокумент24 страницыVidrios y AsbestoOSCAR FABIAN GONZALEZ CASTROОценок пока нет
- Apoyo Hidrostático Con 4 Patines: Manual de La Máquina es-TM - BEA.003.BДокумент61 страницаApoyo Hidrostático Con 4 Patines: Manual de La Máquina es-TM - BEA.003.Bernesto huamanОценок пока нет
- Taller EstequiometricoДокумент5 страницTaller EstequiometricoJoaquin Loza100% (1)
- Materiales de Construccion de Los Equipos de Procesamiento de AlimentoДокумент3 страницыMateriales de Construccion de Los Equipos de Procesamiento de AlimentoYina Martinez Doñez100% (1)