Академический Документы
Профессиональный Документы
Культура Документы
Compuestos-Aromaticos y Alcvoholes Exposicion
Загружено:
Sidalia Mercedes Taveras0%(1)0% нашли этот документ полезным (1 голос)
95 просмотров13 страниц1) Los compuestos aromáticos son hidrocarburos insaturados con una estructura cíclica especial caracterizada por el benceno.
2) El benceno fue el primer compuesto aromático identificado y tiene una estructura cíclica plana propuesta por Kekulé.
3) La regla de Hückel predice si un compuesto cíclico conjugado es aromático o antiaromático basado en el número de electrones p en el anillo.
Исходное описание:
alcoholes
Авторское право
© © All Rights Reserved
Доступные форматы
PPT, PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документ1) Los compuestos aromáticos son hidrocarburos insaturados con una estructura cíclica especial caracterizada por el benceno.
2) El benceno fue el primer compuesto aromático identificado y tiene una estructura cíclica plana propuesta por Kekulé.
3) La regla de Hückel predice si un compuesto cíclico conjugado es aromático o antiaromático basado en el número de electrones p en el anillo.
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате PPT, PDF, TXT или читайте онлайн в Scribd
0%(1)0% нашли этот документ полезным (1 голос)
95 просмотров13 страницCompuestos-Aromaticos y Alcvoholes Exposicion
Загружено:
Sidalia Mercedes Taveras1) Los compuestos aromáticos son hidrocarburos insaturados con una estructura cíclica especial caracterizada por el benceno.
2) El benceno fue el primer compuesto aromático identificado y tiene una estructura cíclica plana propuesta por Kekulé.
3) La regla de Hückel predice si un compuesto cíclico conjugado es aromático o antiaromático basado en el número de electrones p en el anillo.
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате PPT, PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 13
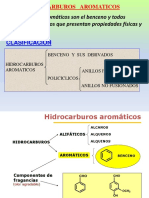
COMPUESTOS AROMATICOS
Los hidrocarburos aromáticos son compuestos insaturados de
un tipo especial. Originalmente recibieron el nombre de
aromáticos debido al aroma que algunos poseen. Sin embargo
no todos son odoríferos y muchos compuestos fragantes no son
de tipo aromático.
Uno de los compuestos más simples y que se conoció primero
con la estructura especial característica de los compuestos
aromáticos fue el hidrocarburo benceno.
NOMENCLATURA
En muchos de los casos de los derivados del benceno , basta con
anteponer el nombre del grupo sustituyente a la palabra benceno
por ejemplo:
Nomenclatura
El sistema IUPAC de nomenclatura para los hidrocarburos
aromáticos conserva un gran número de nombres comunes Así
aunque los compuestos siguientes se podrían nombrar como
bencenos sustituidos , los nombres comunes que se muestran son de
uso casi universal.
Si el anillo bencénico tiene unidos a él más de dos grupos se utilizan
números para indicar sus posiciones relativas, por ejemplo:
Todo benceno disustituido tiene tres isómeros constitucionales, y
existen dos métodos aceptables para escribir la orientación
relativa de los sustituyentes: mediante el uso de números de
posición relativa, y empleando las designaciones orto, meta y para
que se suelan abreviar como o, m y p.
Si los dos grupos son diferentes y ninguno de ellos confiere un grupo
especial a la molécula se nombran sucesivamente y se termina con la
palabra benceno.
Si uno de los dos grupos es del tipo que le da a la molécula un nombre
especial el compuesto se denomina como un derivado de aquella
sustancia especial:
Estructura del benceno
1. 1825, descubierto por Faraday: líquido de p.e. 80ºC
2. 1834, Mitscherlich lo sintetiza y determina su fórmula
molecular C6H6
3. 1866 Kekulé propuso una estructura cíclica de
ciclohexatrieno:
4. No se comporta como insaturado:
- no decolora Br2/Cl4C Br
- no se oxida con KMnO4
Br2
+ H
H
Cl4C
Br
Br
Br2
Br2, FeBr3
HBr + + No hay reacción
Cl4C Cl4C
Regla de Hückel. Comp. aromáticos y
antiaromáticos
Son compuestos
Son compuestos aromáticos los antiaromáticos si cumplen
que los tres primeros criterios,
pero:
cumplen los siguientes criterios:
La deslocalización de
Compuesto cíclicos y electrones p sobre el anillo,
completamente conjugados causa un aumento de la Ep,
siendo menos estable que el
Cada carbono del anillo debe correspondiente compuesto
tener un orbital p no hibridado de cadena abierta. Ej.:
Los orbitales p no hibridados
deben solapar para formar un
anillo continuo de orbitales
paralelos. La estructura debe ser menos estable que
plana o casi plana para que el
solapamiento de los orbitales p
sea efectivo.
La deslocalización de electrones
p origina una disminución de la Ep
(mayor estabilidad) Ej.: benceno
Regla de Hückel (1931) permite predecir cuando un compuesto
cíclico, plano, con dobles enlaces alternados es aromático:
•Si el nº de electrones p es 4n+2, el sistema es aromático
•Si el nº de electrones p es 4n, el sistema es antiaromático
Propiedades físicas y químicas de los
alcoholes
Alcoholes: Se producen al sustituir uno o mas átomos de hidrogeno por
grupos hidroxilo (OH) en los Hidrocarburos saturados y no saturados.
Propiedades físicas:
Solubilidad: La formación de puentes de hidrógeno cuando los oxígenos
unidos al hidrógeno en los alcoholes forman uniones entre sus moléculas y las
del agua permite la asociación entre las moléculas de alcohol. A partir del
hexanol son solubles solamente en solventes orgánicos.
Punto de ebullición: Aumenta con la cantidad de átomos de carbono y
disminuye con el aumento de las ramificaciones.
Punto de fusión: Aumenta a medida que aumenta la cantidad de carbonos.
Densidad: La densidad de los alcoholes aumenta con el número de carbonos
Propiedades químicas:
ESHIDRATDACIÓN: Es una propiedad de los alcoholes mediante la cual
podemos obtener éteres o alquenos.
HALOGENACIÓN: El alcohol reacciona con el ácido hidrácido para formar
haluros de alquilo mas agua.
DESHIDROGENACIÓN: Los alcoholes primarios y secundarios cuando se
calientan en contacto con ciertos catalizadores, pierden átomos de
hidrógeno para formar aldehídos o cetonas.
OXIDACIÓN: La oxidación es la reacción de alcoholes para producir ácidos
carboxílicos, cetonas o aldehídos dependiendo de el tipo de alcohol y de
catalizador.
Вам также может понравиться
- De la estructura atómica a la quiralidad.: Algunos conceptos de la químicaОт EverandDe la estructura atómica a la quiralidad.: Algunos conceptos de la químicaРейтинг: 5 из 5 звезд5/5 (1)
- Hidrocarburos AromaticosДокумент82 страницыHidrocarburos AromaticosCesar AvilaОценок пока нет
- Tarea de UV y FluorescenciaДокумент16 страницTarea de UV y FluorescenciaArturoIvánPavónHernández67% (3)
- QC-12 Quimica OrganicaДокумент24 страницыQC-12 Quimica OrganicaDania Alvo DueñasОценок пока нет
- Formulación Química OrgánicaДокумент94 страницыFormulación Química OrgánicaJeronimo BОценок пока нет
- Informe 6 de Quimica TerminadoДокумент42 страницыInforme 6 de Quimica TerminadoSandraJustino100% (2)
- Introducción A La Síntesis OrgánicaДокумент40 страницIntroducción A La Síntesis OrgánicaWilbert Rivera MuñozОценок пока нет
- Hibridación Del CarbonoДокумент4 страницыHibridación Del CarbonoGilberto Diaz MonroyОценок пока нет
- Aromaticos 14 PDFДокумент45 страницAromaticos 14 PDFOscar CuestasОценок пока нет
- Hidrocarburos Alifáticos y Aromáticos TrabajoДокумент6 страницHidrocarburos Alifáticos y Aromáticos TrabajoRossanaMarquezDiazОценок пока нет
- Guia AromaticosДокумент8 страницGuia AromaticosReyna RomanoОценок пока нет
- BecenosДокумент6 страницBecenosAlex Gutierrez MarquezОценок пока нет
- Clase Tema 1 - Nomenclatura-1Документ37 страницClase Tema 1 - Nomenclatura-1Camila SanchezОценок пока нет
- Tema 2Документ40 страницTema 2liliОценок пока нет
- Compuestos Aromaticos - Quimica OrganicaДокумент64 страницыCompuestos Aromaticos - Quimica OrganicaHarry Alonso Avellaneda LizanaОценок пока нет
- Hidrocarburos AromáticosДокумент7 страницHidrocarburos AromáticosAna Paola Q VОценок пока нет
- Nomenclatura Orgánica - Hidrocarburos Aromáticos (Completo)Документ17 страницNomenclatura Orgánica - Hidrocarburos Aromáticos (Completo)Abel Contreras MaytaОценок пока нет
- Tema 1.1Документ11 страницTema 1.1Yhoselyn MareñoОценок пока нет
- Importante Síntesis de Laboratorio Anillos Aromáticos - 211Документ14 страницImportante Síntesis de Laboratorio Anillos Aromáticos - 211CarlosОценок пока нет
- Los Hidrocarburos y Su ClasificaciónДокумент18 страницLos Hidrocarburos y Su Clasificaciónlourdes peñaОценок пока нет
- Libro Ultimo QuimicaДокумент210 страницLibro Ultimo Quimicaprografic.3020Оценок пока нет
- Guia AromaticosДокумент10 страницGuia AromaticosYolehidis Franchesca Sena VasquezОценок пока нет
- Guia 11°-Quimica Organica IntroduccionДокумент5 страницGuia 11°-Quimica Organica IntroduccionAnselmo Correa HernandezОценок пока нет
- Compuestos - Aromaticos 20-21Документ42 страницыCompuestos - Aromaticos 20-21Manuel GordilloОценок пока нет
- Cap. 15 AromáticosДокумент25 страницCap. 15 AromáticosCésar GastélumОценок пока нет
- Compuestos AromaticosДокумент50 страницCompuestos Aromaticoseuaa_9201100% (6)
- Alcanos, Alquenos y AlquinosДокумент0 страницAlcanos, Alquenos y AlquinosRoberto RivasОценок пока нет
- Hidrocarburos AromaticosДокумент14 страницHidrocarburos AromaticosSidalia Mercedes TaverasОценок пока нет
- Hidrocarburos Aromaticos III 2020Документ11 страницHidrocarburos Aromaticos III 2020Jessenia Ponce VillatoroОценок пока нет
- Compuestos Aromaticos DerivadosДокумент25 страницCompuestos Aromaticos DerivadosAndrea Vivianna Alcalá ValcárcelОценок пока нет
- 11-3 Karol González Taller de Recuperación 4 Periodo QuímicaДокумент11 страниц11-3 Karol González Taller de Recuperación 4 Periodo QuímicaJosé MorenoОценок пока нет
- AromaticidadДокумент6 страницAromaticidadMilagros Valinotti GaunaОценок пока нет
- Informe Hidrocarburos Aromaticos Chamaco Mamani Leslie LisbethДокумент15 страницInforme Hidrocarburos Aromaticos Chamaco Mamani Leslie LisbethJhoselyn Isabel Usmayo QuispeОценок пока нет
- Aromaticidad TautomeriaДокумент11 страницAromaticidad TautomeriaceabymmbtОценок пока нет
- Hidrocarburos AromáticosДокумент82 страницыHidrocarburos AromáticosLuis E Aguilar RОценок пока нет
- Importante Síntesis de Laboratorio para Obtener Anillos Aromáticos - 034Документ21 страницаImportante Síntesis de Laboratorio para Obtener Anillos Aromáticos - 034CarlosОценок пока нет
- HIDROCARBUROS SAT. INSAT y AROMAT.Документ30 страницHIDROCARBUROS SAT. INSAT y AROMAT.Kade CadeОценок пока нет
- Hidrocarburos AromaticosДокумент69 страницHidrocarburos AromaticosElvis Rogers PakitaОценок пока нет
- 18 Hidrocarburos Aromaticos 2019 IfddcДокумент35 страниц18 Hidrocarburos Aromaticos 2019 IfddcDocente Juanpablino 31Оценок пока нет
- Grupos Funcionales 11°Документ12 страницGrupos Funcionales 11°Fredys RivasОценок пока нет
- Unidad III. Introduccion A Los Compuestos OrgánicosДокумент37 страницUnidad III. Introduccion A Los Compuestos Orgánicosabigail.ramirez.herreraОценок пока нет
- AlcanosДокумент14 страницAlcanosSofi SofiОценок пока нет
- Clase Alquenos, Alquinos, AromaticosДокумент21 страницаClase Alquenos, Alquinos, Aromaticosnobody :bОценок пока нет
- Actividad 2. Quimica Informe. HIDROCARBUROS CÍCLICOS Y AROMÁTICOS, HALUROS DE ALQUILO, ALCOHOLES, ÉTERESДокумент13 страницActividad 2. Quimica Informe. HIDROCARBUROS CÍCLICOS Y AROMÁTICOS, HALUROS DE ALQUILO, ALCOHOLES, ÉTERESMara100% (1)
- Funciones Químicas de Los HidrocarburosДокумент13 страницFunciones Químicas de Los HidrocarburosJangel M. LeónОценок пока нет
- Química Del CarbonoДокумент12 страницQuímica Del CarbonoJesus DiazОценок пока нет
- Informe de Laboratorio de Hidrocarburos AromaticosДокумент20 страницInforme de Laboratorio de Hidrocarburos Aromaticosalejandro50% (2)
- Arenos y BencenosДокумент15 страницArenos y BencenosChavaCoconBernardoОценок пока нет
- Clasificacion y Propiedades de Los Compuestos Organicos PDFДокумент16 страницClasificacion y Propiedades de Los Compuestos Organicos PDFJonathan RicoОценок пока нет
- Introducción A La Química OrgánicaДокумент41 страницаIntroducción A La Química OrgánicaIleana GómezОценок пока нет
- Introduccion A La Quimica OrganicaДокумент43 страницыIntroduccion A La Quimica OrganicaQuinterosОценок пока нет
- Compuestos Aromáticos 2Документ9 страницCompuestos Aromáticos 2Betzy Valery Poma PerezОценок пока нет
- Sesión 6. AromáticosДокумент30 страницSesión 6. AromáticosDayana AhumadaОценок пока нет
- Unidad 1.Parte1.QuimicaCompOxi Sept-Oct 2019Документ114 страницUnidad 1.Parte1.QuimicaCompOxi Sept-Oct 2019Luis DominguezОценок пока нет
- Felix Marco Teorico FinalДокумент11 страницFelix Marco Teorico FinalstainОценок пока нет
- Hidrocarburos CiclicosДокумент5 страницHidrocarburos CiclicosMario Tenorio PerezОценок пока нет
- Hidrocarburos AromaticosДокумент120 страницHidrocarburos AromaticosHeidy EspejoОценок пока нет
- Quimica OrganicaДокумент24 страницыQuimica OrganicaPamela SalasОценок пока нет
- Trabajo de Psicologia de La Motivacion AndreaДокумент7 страницTrabajo de Psicologia de La Motivacion AndreaSidalia Mercedes TaverasОценок пока нет
- KeidyДокумент9 страницKeidySidalia Mercedes TaverasОценок пока нет
- Formulario para Control de Agua HidromedДокумент1 страницаFormulario para Control de Agua HidromedSidalia Mercedes TaverasОценок пока нет
- Ley Productos FarmaceuticosДокумент89 страницLey Productos FarmaceuticosSidalia Mercedes TaverasОценок пока нет
- Incentivos PlanificacionДокумент3 страницыIncentivos PlanificacionSidalia Mercedes Taveras0% (1)
- Exposicion Psicologia Analisis de Puestos de TrabajoДокумент17 страницExposicion Psicologia Analisis de Puestos de TrabajoSidalia Mercedes TaverasОценок пока нет
- Lab, de Fluidos Trabajo SidaliaДокумент11 страницLab, de Fluidos Trabajo SidaliaSidalia Mercedes TaverasОценок пока нет
- Ensayo Sobre Ácidos y Bases de Brønsted y LewisДокумент6 страницEnsayo Sobre Ácidos y Bases de Brønsted y Lewissam1974050% (2)
- AminasДокумент45 страницAminasSandyArias67% (3)
- 17 HALOGENOS QuimicaDescriptivaДокумент9 страниц17 HALOGENOS QuimicaDescriptivaSilbana SalgadoОценок пока нет
- Informe AromaticidadДокумент4 страницыInforme AromaticidadMaria Clara RuizОценок пока нет
- Taller 11 ReaccionesДокумент5 страницTaller 11 ReaccionesJaime Cervantes HernandezОценок пока нет
- Compuestos OxigenadosДокумент8 страницCompuestos OxigenadosSamantha Yucra AlfaroОценок пока нет
- H06Документ13 страницH06Adrian VargasОценок пока нет
- Determinacion Del Numero de Moleculas de Agua en Una Sal HidratadaДокумент9 страницDeterminacion Del Numero de Moleculas de Agua en Una Sal HidratadaValeria Perez Estudillo100% (1)
- Trabajo Práctico Integrador Introducción A La QuímicaДокумент10 страницTrabajo Práctico Integrador Introducción A La QuímicaMarisa RobertsОценок пока нет
- La Hibridación Consiste en Una Mezcla de Orbitales Puros en Un Estado Excitado para Formar Orbitales Hibridos Equivalentes Con Orientaciones Determinadas en El EspacioДокумент7 страницLa Hibridación Consiste en Una Mezcla de Orbitales Puros en Un Estado Excitado para Formar Orbitales Hibridos Equivalentes Con Orientaciones Determinadas en El EspacioYamil ValenciaОценок пока нет
- Propiedades Químicas Grupo 16 AnfígenosДокумент17 страницPropiedades Químicas Grupo 16 AnfígenosJuan David Zambrano PerezОценок пока нет
- Pauta Guia de Ejercicios Bonos y AccionesДокумент4 страницыPauta Guia de Ejercicios Bonos y AccionesNicole Troncoso VidalОценок пока нет
- EVALUACION Quimica Organica PDFДокумент5 страницEVALUACION Quimica Organica PDFNoa NatividadОценок пока нет
- Informe 3 Sintesis de WilliamsonДокумент5 страницInforme 3 Sintesis de WilliamsonAngie Gomez100% (1)
- Practica 8 Química de Grupos FuncionalesДокумент12 страницPractica 8 Química de Grupos FuncionalesAle AlvarezОценок пока нет
- 2do Quimica IITДокумент79 страниц2do Quimica IITwgomez_175543Оценок пока нет
- Formato Informe Laboratorio de Quimica IIДокумент12 страницFormato Informe Laboratorio de Quimica IIKevin David AlvarezОценок пока нет
- Desarrollo Histórico de La Química Orgánica Como CienciaДокумент4 страницыDesarrollo Histórico de La Química Orgánica Como CienciaKarlitah Ojeda100% (1)
- Orbitales Moleculares y TCCДокумент2 страницыOrbitales Moleculares y TCCignaciovalenciaОценок пока нет
- Anhidrido MaleicoДокумент10 страницAnhidrido MaleicoAlejandro Vergel UsecheОценок пока нет
- Sustitución Ortho, Meta, y para en Derivados Disustituidos: Química Orgánica Derivados Del Benceno SustituyentesДокумент4 страницыSustitución Ortho, Meta, y para en Derivados Disustituidos: Química Orgánica Derivados Del Benceno SustituyentesLina PérezОценок пока нет
- Fusion Con Sodio InformeДокумент3 страницыFusion Con Sodio InformeYuli SanchezОценок пока нет
- Informe AlcanosДокумент14 страницInforme AlcanosLiseth HumalaОценок пока нет
- BonosДокумент5 страницBonosYeimy Marcela Rubio NavarroОценок пока нет
- Interacciones Moleculares Entre Soluto Y SolventeДокумент2 страницыInteracciones Moleculares Entre Soluto Y SolventeBastosZayasJoseОценок пока нет