Академический Документы
Профессиональный Документы
Культура Документы
Vozmozhnosti Far
Загружено:
Tom0 оценок0% нашли этот документ полезным (0 голосов)
10 просмотров11 страницVozmozhnosti_farmakoterapii_pri_lechenii_gastroenterologicheskikh_zabolevaniy_v_period_beremennosti
Оригинальное название
Vozmozhnosti_far
Авторское право
© © All Rights Reserved
Доступные форматы
PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документVozmozhnosti_farmakoterapii_pri_lechenii_gastroenterologicheskikh_zabolevaniy_v_period_beremennosti
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате PDF, TXT или читайте онлайн в Scribd
0 оценок0% нашли этот документ полезным (0 голосов)
10 просмотров11 страницVozmozhnosti Far
Загружено:
TomVozmozhnosti_farmakoterapii_pri_lechenii_gastroenterologicheskikh_zabolevaniy_v_period_beremennosti
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 11
Обзоры и лекции
© ЦИММЕРМАН Я.С., МИХАЛЕВА Е.Н. 2015
УДК 618.3-06:616.3-085.24
ВОЗМОЖНОСТИ ФАРМАКОТЕРАПИИ ПРИ ЛЕЧЕНИИ
ГАСТРОЭНТЕРОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ В ПЕРИОД БЕРЕМЕННОСТИ
Циммерман Я.С.1, Михалева Е.Н.2
1
ГБОУ ВПО «Пермский государственный медицинский университет им. акад. Е.А. Вагнера», 614990, г. Пермь;
2
ГБУЗ «Городская клиническая больница № 2 им. Ф.Х. Граля», г. Пермь
Для корреспонденции: Циммерман Яков Саулович — д-р мед. наук, проф.; тел. 8(342) 281-27-74
В статье изложены современные представления о тактике ведения и терапевтических возможностях в лечении
основных гастроэнтерологических заболеваниях в период беременности. Указаны особенности течения ряда за-
болеваний пищеварительного тракта в период беременности и влияние обострения хронических болезней органов
пищеварения на процесс вынашивания плода. Представлены наиболее распространенные болезни пищеварительной
системы: гастроэзофагеальная рефлюксная болезнь, болезни желудка и двенадцатиперстной кишки, острые и хро-
нические панкреатиты, бескаменный и калькулезный холециститы, гепатиты различной этиологии, в том числе
аутоиммунный, циррозы печени и воспалительные заболевания кишечника. Приведены возможности и особенности
лекарственной терапии в период беременности при обострении основных гастроэнтерологических заболеваний.
К л ю ч е в ы е с л о в а: беременность; заболевания пищеварительной системы; лекарственная терапия; терато-
генный эффект; эмбриотоксический эффект.
Для цитирования: Клин. мед. 2015; 93 (8): 8—18.
POSSIBILITIES FOR PHARMACOTHERAPY OF GASTROENTEROLOGICAL DISEASES DURING PREGNANCY
Tsimmerman Ya.S., Mikhaleva E.N.
E.A. Vagner Perm State Medical University, Perm; F.Kh. Gral’ City Clinical Hospital No 2, Perm, Russia
Correspondence to: Yakov S. Tsimmerman - MD, PhD, DSc, prof.
Modern views of the strategy for the treatment of the main gastroenterological diseases during pregnancy are considered.
Peculiarities of the clinical course of digestive tract pathologies are discussed with reference to the influence of exacerbation
of their chronic forms on fetus development. The most common gastroenterological pathologies include gastroesophageal
reflux disease, gastric and duodenal disorders, acute and chronic pancreatitis, acalculous and calculous cholecystitis, hepatitis
of autoimmune and other etiology, liver cirrhosis, intestinal inflammation. Possibilities of pharmacotherapy and its specific
features in pregnant women are discussed including cases of exacerbation of chronic conditions.
K e y w o r d s: pregnancy; digestive disorders; pharmacotherapy; teratogenic effect; embryotoxic effect.
Citation: Klin. med. 2015; 93 (8): 8—18. (in Russian)
В последние годы возможности фармакотерапии способных вызвать нарушения в развитии эмбриона и
гастроэнтерологических заболеваний многократно плода [1, 2]. Особенно это стало очевидным после из-
возросли. Поэтому многие хронические заболевания, вестной талидомидовой трагедии. Напомним кратко ее
при которых еще недавно беременность была нежела- историю.
тельной или невозможной, сегодня успешно поддаются В 1959—1960 гг. в странах Западной Европы и в
лечению и не являются препятствием к рождению ре- Австралии появились сообщения об участившихся
бенка. Кроме того, необходимо учитывать, что сегодня случаях рождения детей с уродствами. Первоначаль-
многие женщины предпочитают рожать после 30 лет, а но повышение частоты врожденных пороков разви-
с возрастом растет частота различных заболеваний и, тия пытались связать с вирусной инфекцией, иони-
следовательно, потребность в медикаментозном лече- зирующей радиацией, которые способны нарушить
нии. При этом наиболее частыми хроническими болез- эмбриогенез, однако вскоре удалось установить, что
нями у беременных являются именно заболевания пи- появление уродств у детей обусловлено приемом бе-
щеварительной системы, на долю которых приходится ременными нового снотворного средства — пре-
до 10% всех случаев [1, 2]. парата талидомида, который уже на ранних сроках
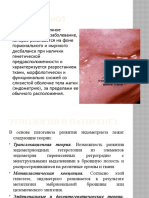
При лечении женщин в период беременности и лак- беременности обусловливал развитие у плода свое-
тации необходимо учитывать также влияние медика- образных уродств верхних и нижних конечностей, ко-
ментов на плод. Лекарственные препараты занимают торые по внешнему виду напоминали ласты тюленя.
одно из ведущих мест среди факторов внешней среды, В связи с этим эту аномалию развития назвали фокоме-
8 КЛИНИЧЕСКАЯ МЕДИЦИНА, № 8 , 2015
лией (от греч. рhoke — тюлень, melos — часть тела, дозреваемые в том, что они могут их вызвать. Следует
конечность). Фокомелия, как правило, сопровождалась соотносить риск их приема для плода с потенциальной
аномалиями развития внутренних органов и систем пользой от применения лекарственного препарата.
организма. В течение короткого промежутка времени Категория Х — лекарства с высоким риском по-
число таких детей в разных странах достигло несколь- явления врожденных пороков развития или стойких
ких тысяч. повреждений плода с доказанным тератогенным или
Следует отметить, что сама по себе токсичность та- эмбриотоксическим действием как у животных, так и
лидомида невелика. И на организм взрослого человека у человека. Их применение во время беременности не-
талидомид оказывает даже менее отчетливое побочное допустимо.
действие, чем другие широко распространенные снот- По этическим соображениям контролируемые ис-
ворные средства (нембутал, веронал). В опытах на жи- следования у беременных практически не проводятся,
вотных в период беременности талидомид не оказывал поэтому их абсолютная безопасность не гарантирована
тератогенного действия, однако, несмотря на свою не- [2, 7]. Во время беременности могут применяться только
большую токсичность, талидомид обладал избиратель- те лекарственные препараты, особенности метаболизма
ной способностью нарушать процесс эмбриогенеза у которых точно установлены. Они не оказывают повреж-
человека. Поражал тот факт, что физические уродства у дающего воздействия на эмбрионы приматов и хорошо
детей, связанные с приемом талидомида, могли переда- зарекомендовали себя в клинической практике [5, 7].
ваться по наследству. Описаны случаи, когда у дочерей При беременности в организме женщины происхо-
женщин, принимавших талидомид, рождались дети дят обратимые физиологические изменения, связан-
с укороченными конечностями. Изложенные факты ные с нейроэндокринными и обменными процессами.
стали мощным стимулом для всестороннего изучения В биохимическом анализе крови определяются следу-
проблемы воздействия лекарственных препаратов на ющие изменения [8—10].
развитие плода [3]. Содержание общего белка (норма 63—83 г/л) может
В 2005 г. в Лондоне на Трафальгарской площади незначительно уменьшаться (53—63 г/л), что не являет-
Марк Куинн установил памятник жертвам талидомида. ся патологией и связано с увеличением общего объема
В качестве модели выступала Эллисон Леппер, которая плазмы и уменьшением количества эритроцитов.
на момент создания памятника была беременна. К сча- Уровень холестерина (норма 3,15—5,8 ммоль/л) мо-
стью, ее ребенок родился здоровым. жет повышаться до 6,2 ммоль/л, что обусловлено уве-
Следует заметить, что от талидомида не пострадали личением образования эндогенного холестерина, не-
беременные в двух ведущих державах мира — СССР и обходимого для формирования сосудистого русла пла-
США, хотя в обеих странах этот препарат уже проходил центы и плода.
регистрацию. В этот период Федеральное управление по Уровень глюкозы (норма 3,9—5,8 ммоль/л) может
контролю за качеством продуктов питания и лекарствен- незначительно снижаться (до 3,5 ммоль/л) в связи с воз-
ных препаратов США (Food and Drug Administration — растанием ее потребления плодом.
FDA) приняло решение разделить по безопасности все Активность щелочной фосфатазы (норма до 150 Ед/л)
лекарственные средства, применяемые в период бере- при беременности может повышаться в 2—4 раза, по-
менности, на 5 категорий: A, B, C, D, X [4—6]. скольку плацента является ее дополнительным источ-
Категория А — лекарства, которые принимаются ником.
большим количеством беременных без каких-либо до- Уровень креатинина (норма 53—97 мкмоль/л) может
казательств их влияния на частоту врожденных анома- снижаться до 35—70 мкмоль/л вследствие увеличения
лий или повреждающего действия на плод. объема крови, почечного плазмотока и фильтрации.
Категория В — лекарства, которые принимаются Содержание аланинаминотрансферазы, аспартата-
ограниченным количеством беременных без каких-ли- минотрансферазы (АСТ), амилазы, билирубина, моче-
бо доказательств их влияния на частоту врожденных вины, микроэлементов не изменяется.
аномалий или повреждающего действия на плод. В ис- Биохимический анализ крови необходимо выпол-
следованиях на животных не выявлено повышения ча- нять дважды: при постановке беременных на учет и
стоты повреждений плода или такие результаты полу- при 30-недельной беременности. При сроке беременно-
чены, но доказательств их зависимости от применения сти 24—28 нед рекомендуется дополнительное иссле-
препарата не выявлено. дование уровня глюкозы в крови. В этот период отме-
Категория С — лекарства, которые в исследованиях чается повышенная потребность организма в инсулине,
на животных продемонстрировали тератогенное или что может превысить функциональные возможности
эмбриотоксическое действие. Есть основания предпо- эндокринной ткани поджелудочной железы, вырабаты-
ложить, что они могут оказывать обратимое отрица- вающей инсулин, с развитием гестационного сахарного
тельное воздействие на плод или на новорожденного, диабета.
однако не приводят к появлению врожденных пороков В общем анализе крови также происходят опреде-
развития. ленные изменения: повышается уровень гемоглоби-
Категория D — лекарства, вызывающие аномалии на, увеличиваются количество эритроцитов, объем
развития или необратимые повреждения плода, или по- плазмы крови и объем циркулирующей крови. Отме-
КЛИНИЧЕСКАЯ МЕДИЦИНА, № 8, 2015 9
чается небольшой нейтрофильный лейкоцитоз, СОЭ сосредоточены главным образом у берегов Норвегии.
повышается до 30 мм/ч. Наблюдаются изменения и в Преимуществом альгинатов перед антацидами являет-
свертывающей системе крови: увеличивается содержа- ся полное отсутствие системного действия, механизм
ние фибриногена, протромбина, факторов V, VI, VIII, которого имеет физическую природу. Гевискон не вли-
X. Возрастает адгезивность тромбоцитов. Антикоагу- яет на консистенцию стула, а, как известно, до 15—30%
лянтный потенциал крови и фибринолитическая актив- антацидов, содержащих соли магния и алюминия, мо-
ность плазмы снижаются [11, 12]. гут всасываться после реакции с соляной кислотой; при
Беременность оказывает влияние и на функци- этом соли алюминия усиливают запор, а сульфат маг-
ональное состояние пищеварительной системы. За ния может привести к слабости родовой деятельности и
счет снижения чувствительности хеморецепторов к появлению судорог. Кроме того, альгинаты оказывают
серотонину и гистамину происходит снижение пери- более длительное (до 4—4,5 ч) действие. Гевискон фор-
стальтической активности кишечника. Под влиянием те не влияет на биодоступность других препаратов, не
прогестерона снижается тонус гладкой мускулатуры нарушает их всасывания, не взаимодействует с ними,
желудочно-кишечного тракта. Растущая матка способ- не оказывает тератогенного влияния [7, 19, 22].
ствует повышению внутрибрюшного давления и дис- Во время беременности возможно назначение бло-
координации тонуса толстой кишки, а замедление кро- каторов Н2-гистаминовых рецепторов — ранитидина и
вотока в воротной и нижней полой венах и полнокровие фамотидина (отнесены FDA к категории В) [5, 24]. Это
геморроидальных вен обусловливают дисфункцию ки- часто назначаемая группа препаратов, всесторонне из-
шечника. Кроме того, увеличивается провоспалитель- ученная и наиболее безопасная. Имеется достаточно
ный потенциал мезенхимальных тканей, что приводит клинических данных, свидетельствующих о безопас-
к обострению ранее существовавших воспалительных ности ранитидина (по 150 мг 2 раза в сутки) [24].
процессов [11, 13, 14]. Ингибиторы протонной помпы (ИПП) — наиболее
Поводом для обращения беременных к врачу чаще действенный класс препаратов при лечении кислото-
всего являются следующие гастроэнтерологические зависимых заболеваний, однако их влияние на плод
заболевания: гастроэзофагеальная рефлюксная бо- изучено недостаточно, поэтому их назначают только
лезнь (ГЭРБ); обострение хронического гастрита (ХГ) при подтвержденных и эндоскопически выраженных
и язвенной болезни (ЯБ); хронический панкреатит или осложненных формах ГЭРБ [25]. Омепразол отне-
(ХП); острый панкреатит (ОП); заболевания гепато- сен FDA к категории С [5]. Пантопразол, рабепразол и
билиарной системы; воспалительные заболевания ки- эзомепразол включены FDA в категорию В [5], однако
шечника (ВЗК). об их влиянии на беременных имеется мало данных и
Гастроэзофагеальная рефлюксная болезнь. Не- не исключается их токсическое влияние на плод. При
которые авторы рассматривают изжогу у беременных выборе ИПП следует ориентироваться на более дли-
как неспецифический симптом, появляющийся на фоне тельное клиническое использование препарата, когда
беременности и обусловленный ею, который самосто- имеется возможность ретроспективно оценить отсут-
ятельно купируется после родоразрешения. На изжо- ствие тератогенного или эмбриотоксического действия
гу жалуется только 5% беременных. ГЭРБ занимает [25, 26]. Кроме того, при выборе всегда следует пред-
2-е место среди всех болезней органов пищеварения почитать оригинальные препараты, так как они лучше
и встречается, по данным разных авторов, в 21—80% изучены, в то время как дженерики могут отличаться
случаев [15, 16]. Целью лечебных мероприятий при по биоэквивалентности, клинической эффективности,
ГЭРБ является максимальное снижение агрессивного содержанию вспомогательных веществ и наличию по-
кислотно-пептического фактора. При незначительно вы- бочных эффектов [27]. На сегодняшний день на фар-
раженной изжоге для купирования клинической сим- мацевтическом рынке представлен лишь один ИПП,
птоматики достаточно изменения стиля жизни (lifestyle официально разрешенный к применению во время
modification), режима питания, соблюдения диеты и беременности и лактации, это лосек МАПС — ориги-
нормализации стула (коррекция запора) [15—19]. нальный омепразол, созданный фирмой AstraZeneca
При необходимости медикаментозного лечения на- (Швеция) более 25 лет назад [28]. Кроме того, он явля-
значают невсасывающиеся антациды (магний-, алюми- ется одним из немногих препаратов, действие которого
ний- или кальцийсодержащие): маалокс, фосфалюгель и изучалось во время беременности. Установлено, что
др. Антациды быстро купируют изжогу, но их действие его использование в терапевтических дозах в любом
продолжается только 40—60 мин. В исследованиях на триместре беременности не повышает риска возникно-
животных антациды доказали отсутствие тератогенно- вения пороков развития у плода [27—30]. Назначается
го воздействия [20—23]. Более эффективны альгинаты препарат в дозе 20—40 мг /сут; курс 4—8 нед.
(гевискон), которые получают из морских водорослей Прокинетики, используемые при лечении ГЭРБ,
(Laminaria hyperborea). Они образуют плотные гели, обусловливают существенное облегчение диспепси-
создающие механический барьер-плот, препятствую- ческих симптомов, однако разрешен к применению в
щий воздействию соляной кислоты и щелочи на сли- гестационный период только метоклопрамид, который
зистую оболочку пищевода [7, 13, 15, 22]. В глобальном отнесен FDA к категории В [5, 7]. Назначается препарат
масштабе запасы этих водорослей ограничены: они в дозе 10 мг 3 раза в сутки.
10 КЛИНИЧЕСКАЯ МЕДИЦИНА, № 8 , 2015
Хронический гастрит и язвенная болезнь. Обо- холелитиаза в связи с часто наблюдающимся при бере-
стрение ХГи ЯБ не влияет на процесс вынашивания менности нарушением моторно-эвакуаторной функции
и рождения ребенка. Беременность даже «смягчает» желчного пузыря (гипокинез, спазм сфинктера Одди),
течение ЯБ: у большей части женщин наблюдается ре- повышением вязкости желчи и концентрации холесте-
миссия ЯБ [13], что связано со снижением кислотности рина, увеличением общего содержания желчных кис-
и повышением образования слизи в период беременно- лот. Это приводит к нарушению их энтерогепатической
сти, уменьшением моторно-эвакуаторной активности циркуляции и уменьшению соотношения хенодезокси-
желудка, усилением кровотока и гиперпродукцией по- холевой и холевой кислот. У 30% женщин к началу III
ловых гормонов (эстрогены повышают интенсивность триместра беременности при ультразвуковом исследо-
регенераторных процессов в тканях). Обострение ЯБ вании определяется наличие билиарного сладжа, а у
возможно в I или III триместре (на 36—38-й неделе) 12% — камней [33]. Еще одной причиной обострения
беременности. Часто обострению ХГ и ЯБ сопутствует ХП во время беременности является гиперлипидемия,
развитие раннего токсикоза [17, 31]. Медикаментозная гипертриглицеридемия, особенно при наличии ожире-
терапия проводится только при отсутствии эффекта ния и метаболического синдрома [33, 34]. Максималь-
от соблюдения режима питания, диеты, при неэффек- ное повышение уровня триглицеридов и липопротеинов
тивности невсасывающихся антацидов или альгинатов в сыворотке крови отмечено в III триместре беременно-
или при развитии осложнений. Эрадикационная те- сти, когда наблюдается учащение случаев обострения
рапия инфекции Helicobacter pylori противопоказана. ХП [35]. Определенное значение в обострении ХП при
Возможно назначение ранитидина или лосека МАПС в беременности имеет гиперпаратиреоз, который в той
обычных терапевтических дозах. Кроме того, в период или иной мере присутствует при нормально протека-
беременности может быть рекомендовано назначение ющей беременности и сопровождается увеличением
гастропротектора сукральфата (вентер), который отне- содержания внутриклеточного кальция с образованием
сен FDA к категории В [5]. Его действие оценивалось кальцинатов, обтурирующих панкреатические протоки.
в рандомизированных плацебо-контролируемых ис- Способствовать обострению ХП может и прием таких
следованияхс участием беременных [32, 33]. Препарат лекарственных препаратов, как тиазидные диуретики,
принимают по 1 г 4 раза в сутки за 1 ч до еды в течение метронидазол, витаминно-минеральные комплексы,
10—14 дней. Препараты висмута (де-нол, бисмофальк) препараты кальция, железа, сульфасалазин, глюкокор-
отнесены FDA к категории С [5], поскольку возможно тикостероиды (ГКС) [33, 36] . Полагают, что появление
токсическое влияние висмута на плод, поэтому при- симптомов диспепсии в первые 12 нед связано с самой
ем этих препаратов при беременности не рекоменду- беременностью, а после 12 нед является поводом для
ется. М-холинолитики также отнесены FDA к катего- обследования на наличие ХП [37].
рии С; кроме того, они уступают по силе действия Н2- Острый панкреатит. Возникновение ОП при бере-
блокаторам гистаминовых рецепторов и ИПП, поэтому менности сроком до 12 нед определяет необходимость
при беременности не используются [5]. Миотропные ее прерывания, а при сроке более 36 нед — досрочного
спазмолитики но-шпа и папаверин, напротив, приме- родоразрешения. При возникновении угрозы прерыва-
няются в любые сроки беременности в общетерапевти- ния беременности на любом сроке сохранять ее в слу-
ческих дозах [2]. Допускается использование дюспата- чае развития ОП нецелесообразно. При необходимо-
лина при положительном соотношении риска для плода сти хирургического лечения осложнений ОП вначале
и пользы для матери. Препарат избирательно снижает производят кесарево сечение, причем, если оно вы-
тонус гладкой мускулатуры органов пищеварения, не полняется при наличии перитонита, операция долж-
оказывая влияния на матку и сосуды [2, 31]. Кроме того, на завершаться ампутацией матки. Перинатальная
дюспаталин расслабляет сфинктер Одди, который ре- смертность плода в этом случае достигает 30—45%
гулирует поступление желчи и поджелудочного сока в [38]. Лечение при ОП проводится в палате интенсив-
двенадцатиперстную кишку. Поскольку у беременных ной терапии. Назначают голод на 2—3 дня, при необ-
сфинктер Одди часто спазмирован, возникает спасти- ходимости — парентеральное питание с последующим
ческая боль. Препарат принимают по 200 мг 2 раза в строгим ограничением жиров и продуктов, богатых
сутки — за 20 мин до завтрака и до ужина. кальцием. Оправдано назначение октреотида (при стой-
Хронический панкреатит. ХП не является проти- ком болевом синдроме и гиперферментемии) по 50—
вопоказанием для беременности и существенно не вли- 100 мкг подкожно 3 раза в сутки в течение 3—5 дней.
яет на ее течение и исход. При отсутствии выраженных Со II триместра беременности возможно назначение
клинических признаков обострения ХП не нарушает контрикала (до 60 000 Ед/сут). ИПП назначают па-
фетоплацентарного гомеостаза [2, 32]. Вместе с тем бе- рентерально: лосек МАПС по 40 мг внутривенно в 100
ременность предрасполагает к обострению ХП, причем мл физиологического раствора. После стабилизации
наиболее частой причиной обострения является соче- процесса переходят на пероральный прием препарата
танная с ХП билиарная патология (сладж, холелитиаз) по 20 мг 2 раза в сутки. Коррекция водно-электролит-
[33] . Как известно, во время беременности создаются ного баланса проводится из расчета 40 мл на 1 кг мас-
условия как для клинической манифестации имеюще- сы тела при соотношении коллоидов и кристаллоидов
гося калькулезного холецистита, так и для развития 1:4. Для предупреждения инфекционных осложнений
КЛИНИЧЕСКАЯ МЕДИЦИНА, № 8, 2015 11
используют полусинтетические пенициллины или це- • острой жировой дистрофией печени беременных;
фалоспорины III—IV поколения. Борьбу с отеком под- • поражением печени при преэкласпсии и экламп-
желудочной железы проводят с помощью фуросемида сии;
или маннитола. Кроме того, назначают миотропные • HELP-синдромом.
спазмолитики (дротаверин, папаверин, дюспаталин) и 2. Поражения печени, не обусловленные беременно-
анальгетики (анальгин, кеторол, трамадол, промедол). стью.
Морфин при беременности строго противопоказан, так А. Острые заболевания, развивающиеся во время
как вызывает угнетение дыхательного центра плода и беременности:
формирует у него лекарственную зависимость. • острый гепатит (вирусный, лекарственный, токси-
При обострении ХП лечение проводится в стаци- ческий);
онарах терапевтического профиля [31, 33]. Назначают • острый холестаз, обусловленный билиарной об-
строгую диету с ограничением жиров, а также про- струкцией;
дуктов, богатых кальцием и растительной клетчаткой. • синдром Бадда — Киари.
Применяются ИПП (лосек МАПС по 20 мг 2 раза в сут- Б. Хронические заболевания печени, предшествую-
ки), антациды или альгинаты (гевискон). Миотропные щие беременности:
спазмолитики и анальгетики назначают парентераль- • хронические гепатиты разной этиологии;
но. Можно использовать 0,5% раствор новокаина (по • цирроз печени (ЦП);
50 мл внутривенно капельно) в 5% растворе глюкозы • тромбоз воротной вены;
(200 мл). При стихании обострения ХП спазмолитики • состояние после трансплантации печени.
заменяют на прокинетики (метоклопрамид). При кли- Во время беременности течение ряда заболеваний
нически значимом дисбиозе тонкой кишки (синдром печени и желчевыводящих путей приобретает некото-
избыточного бактериалього роста) можно использо- рые особенности, что требует использования опреде-
вать рифаксимин или нифуроксазид в терапевтических ленной лечебной тактики.
дозах. Кроме того, рекомендуется полиферментная те- Течение хронического бескаменного холецистита не
рапия (креон по 25 000 — 40 000 ЕД). Контроль выра- претерпевает особенных изменений и не вредит плоду,
женности внешнесекреторной недостаточности подже- поэтому не является показанием для прерывания бере-
лудочной железы проводят путем определения концен- менности; хронический бескаменный холецистит чаще
трации эластазы-1 в кале. обостряется в III триместре беременности.
Заболевания гепатобилиарной системы. Размер При калькулезном холецистите беременность спо-
печени и селезенки при нормально протекающей бере- собствует как образованию и росту желчных камней,
менности не изменяется. У 60% женщин в конце II — так и появлению клинических симптомов ранее скрыто
начале III триместра беременности могут появлять- протекавшего холелитиаза [33]. Обострения чаще про-
ся кожные печеночные знаки: пальмарная эритема, исходят во II триместре беременности. При неэффек-
телеангиэктазии на груди, лице, шее, что обусловле- тивности консервативной терапии в течение недели
но гиперэстрогенемией и повышением внутрибрюш- показано оперативное лечение. На поздних сроках бе-
ного давления в связи с ростом беременной матки и ременности холецистэктомии предшествует родораз-
повышением портального венозного давления. Эти решение.
кожные проявления исчезают в течение 1—2 мес по- Острый вирусный гепатит А у беременных как по
сле родов [39]. Гистологическое исследование печени длительности инкубационного периода, так и по кли-
во время беременности, как правило, не выявляет па- ническому течению не отличается от вирусного гепа-
тологических изменений [40]. Во время беременности тита А вне беременности. При этом инфицирования
развивается умеренный холестаз, возникающий под плода и новорожденного не происходит.
влиянием эстрогенов и протекающий с увеличением Острые вирусные гепатиты В и С протекают тяже-
содержания желчных кислот, холестерина, тригли- лее и сопровождаются более длительным периодом
церидов, щелочной фосфатазы. Отмечается незначи- желтухи, интоксикацией, печеночной энцефалопатией.
тельное снижение концентрации общего белка и аль- Возможно заражение новорожденного, если на его коже
буминов. В то же время синтез других белков в печени есть ссадины или повреждения [8—10].
увеличивается, что находит отражение в повышении Наличие у женщины вирусов гепатита В и С не вли-
уровня γ-глобулинов, церулоплазмина, трансферрина, яет на ее репродуктивную функцию, не повышает ри-
фибриногена и других факторов свертывания крови. ска мертворождения и врожденных аномалий, однако
Нормализация всех этих показателей происходит че- риск инфицирования ребенка при наличии у матери
рез 4—6 нед после родов [8—10]. маркера вирусного гепатита В достигает 80—90%. При
Классификация патологических состояний пече- отсутствии этого маркера в крови матери риск снижа-
ни у беременных [8—10, 39]. ется до 2—15%. При этом не возникает оснований для
Поражения печени, обусловленные беременностью выполнения кесарева сечения с целью снижения риска
и проявляющиеся: инфицирования ребенка. Во время родов рекоменду-
• рвотой беременных; ется избегать амниоцентеза, применения акушерских
• внутрипеченочным холестазом беременных; щипцов, а также длительного безводного периода.
12 КЛИНИЧЕСКАЯ МЕДИЦИНА, № 8 , 2015
Грудное вскармливание не является противопоказани- должна быть продолжена. Доза препарата может быть
ем при условии целостности сосков [41—46]. снижена в III триместре беременности, поскольку воз-
Беременность способна усугубить течение ЦП, ко- растает потребление меди плодом. Кроме того, возмо-
торый в свою очередь неблагоприятно влияет на те- жен временный перевод на поддерживающую терапию
чение и исход беременности. Роды и послеродовый препаратами цинка, которые менее опасны для плода,
период у этих больных часто сопровождаются кро- чем D-пеницилламин. Грудное вскармливание при ле-
вотечением. Беременность при ЦП противопоказана чении D-пеницилламином противопоказано [46, 56, 57].
[47—49], однако при настойчивом желании она может При вирусных гепатитах противовирусная терапия
быть сохранена, если заболевание не сопровождается (ПВТ) во время беременности не проводится. Препара-
признаками декомпенсации и выраженной портальной ты интерферона FDA отнесены к категории С, рибаве-
гипертензией, а варикозное расширение вен пищевода рин — к категории Х [5]. В случае наступления бере-
не превышает I степени. Следует иметь в виду, что во менности на фоне проводимой ПВТ нет необходимости
II триместре беременности варикозное расширение вен в прерывании беременности, но ПВТ должна быть пре-
пищевода и портальная гипертензия могут нарастать кращена. Зачатие может быть рекомендовано не ранее
вследствие увеличения объема крови. чем через 6 мес после окончания лечения этими пре-
Аутоиммунные заболевания печени (АИЗП) — ау- паратами [46, 58, 59].
тоиммунный гепатит (АИГ), первичный билиарный При выборе гепатопротекторов необходимо учиты-
цирроз (ПБЦ) и первичный склерозирующий холангит вать показатели биохимического анализа крови и кли-
(ПСХ) не включены в перечень медицинских показаний ническую ситуацию.
к искусственному прерыванию беременности, и этот Эссенциальные фосфолипиды (ФЛ) восполняют де-
вопрос должен решаться индивидуально [50]. Высокая фицит ФЛ клеточной стенки, стабилизируют мембра-
активность АИЗП сопровождается гипогонадизмом, ны гепатоцитов, уменьшают процесс цитолиза. Кроме
аменореей и бесплодием. Поэтому наступление бере- того, они оказывают антиоксидантное действие, уча-
менности возможно лишь на ранних стадиях АИЗП и ствуя в реакциях перекисного окисления липидов, но
на фоне адекватно проводимой фармакотерапии [51, 52]. им присущи недостатки. Так, часто не удается приоста-
Беременность протекает в состоянии естественной им- новить воспалительный процесс путем назначения ФЛ
муносупресии и может оказать иммуномодулирующее извне, если не устранены патогенетические механиз-
действие на течение всех аутоиммунных заболеваний. мы повреждения. Отсутствуют доказательства того,
Благодаря этому обострений АИГ на фоне беременно- что экзогенные ФЛ растительного происхождения
сти чаще всего не бывает, а биохимические показатели способны «встроиться» в мембрану животной клетки,
даже улучшаются [53]. Нормальное завершение бере- отсутствуют достоверные данные, подтверждающие
менности при АИГ наблюдается у большинства (74%) их эффективность при болезнях печени (степень дока-
женщин [51]. Реже возникает ухудшение состояния, на- зательности D — мнение экспертов). Отмечена низкая
растает активность процесса в печени с развитием пе- биодоступность ФЛ, которые, поступая в лимфатиче-
ченочной недостаточности, гестоза, фетоплацентарной скую систему или кровяное русло, накапливаются в
недостаточности, отслойки нормально расположенной других органах и тканях, не достигая печени.
плаценты, кровотечений. Вероятность обострения АИГ В России эссенциальные ФЛ применяются часто,
выше в первой половине беременности и послеродовом в то время как в Европе и США они не используют-
периоде. Патология плода в этих случаях проявляется ся в клинической практике, поскольку проведенное в
в гипотрофии, признаках внутриутробной гипоксии и 2003 г. рандомизированное плацебо-контролируемое
недоношенности [53—55]. По мере прогрессирования исследование не выявило положительного влияния эс-
заболевания и формирования ЦП повышается частота сенциальных ФЛ на функции печени по сравнению с
самопроизвольного прерывания беременности и вну- плацебо. Напротив, было установлено, что при острых
триутробной смерти плода. Перинатальная смертность и хронических вирусных гепатитах эссенциальные ФЛ
может достигать 64,5% [47]. В то же время на ранних противопоказаны, так как они могут способствовать
стадиях ПБЦ и ПСХ беременность чаще протекает без усилению холестаза и цитолиза [60]. В качестве лекар-
осложнений. Нарастание холестаза при ПБЦ или ПСХ ственных препаратов эссенциальные ФЛ зарегистри-
на фоне беременности ассоциируется с риском невына- рованы только в странах СНГ, а в Европе и США они
шивания беременности и мертворождения [52, 56]. используются лишь как пищевые добавки.
Болезнь Вильсона развивается в молодом возрасте и Хофитол — экстракт листьев артишока полевого яв-
часто сопровождается бесплодием и самопроизвольны- ляется фитогепатопротектором, дает антиоксидантный,
ми абортами [39]. Однако современная медьэлимини- холеретический и диуретический эффекты, улучшает
рующая терапия препаратами D-пеницилламина (отне- дезинтоксикационную функцию печени, способствует
сены FDA к категории D) [5] и цинка приводит к вос- нормализации липидного обмена, уменьшает содер-
становлению функции печени, а также репродуктивной жание мочевины в крови. К достоинствам препарата
функции. Отмена приема D-пеницилламина при насту- относятся эффективность при синдроме цитолиза, со-
плении беременности может привести к опасному для четанных заболеваниях печени и почек и токсикозах бе-
жизни матери обострению процесса, поэтому терапия ременных (улучшается детоксикационная функция пе-
КЛИНИЧЕСКАЯ МЕДИЦИНА, № 8, 2015 13
чени). Кроме того, у хофитола практически отсутствуют лирующее (уменьшает продукцию провоспалительных
побочные эффекты. Отмечены следующие недостатки. цитокинов, подавляет аутоиммунные процессы), анти-
Стимуляция метаболических процессов может приве- токсическое, гипохолестеринемическое (уменьшает
сти к активации хронического гепатита и ЦП, поэтому насыщение желчи холестерином за счет угнетения его
применение фитогепатопротекторов нежелательно при абсорбции в кишечнике, подавления синтеза в печени
выраженной активности процесса. Желчегонный эф- и уменьшения секреции в желчь), противоопухолевое
фект, присущий хофитолу, может усугубить проявления (предотвращает специфические для рака толстой киш-
холестаза, поэтому препарат противопоказан при холе- ки клеточные мутации, стимулирует апоптоз в слизи-
литиазе, острых холециститах и гепатитах [61, 62]. стой оболочке толстой кишки) действие и влияет на
Хофитол может применяться во время беременно- печень и нервную систему (торможение апоптоза, ней-
сти и лактации под контролем врача по 2—3 таблетки ропротекторное действие) [66].
внутрь 3 раза в сутки перед едой в течение 2—3 нед. Впервые УДХК была обнаружена в желчи бурых
Адеметионин (гептрал) является природным анти- медведей в Китае в 1902 г. Медвежья желчь исполь-
оксидантом и антидепрессантом. Препарат дает холе- зовалась в лечебных целях в тибетской, китайской,
ретический и холекинетический эффекты, нормализует корейской и старославянской медицине. Ее применя-
моторику желчевыводящих путей. Он эффективен как ли при желтухе, дизентерии, болезнях печени, глаз,
при гепатоцеллюлярном, так и при каналикулярном хо- использовали для остановки кровотечений. В 1954 г.
лестазе, протекающем на фоне вирусных, алкогольных, японский ученый T. Kanasawa описал синтез УДХК из
лекарственных, токсических поражений печени [61, желчи, а в 1957 г. был создан первый препарат УДХК,
63—65]. Эффективен гептрал и при холестазе беремен- содержащий желчь бурых медведей, — Урсо 100
ных (III триместр). К достоинствам гептрала относятся (1 капсула содержала 100 мг УДХК). В России этот
возможность парентерального введения; высокая био- препарат был зарегистрирован, но в страну практиче-
доступность; антидепрессивный эффект; опосредован- ски не поставлялся. В 1979 г. в Германии был синте-
ное антифибротическое действие. Имеются и недостат- зирован урсофальк, который считается референтным
ки. Так, известны лишь единичные рандомизирован- препаратом: все формы УДХК сравниваются по био-
ные исследования (степень доказательности С), причем эквивалентности именно с ним [60, 71]. К достоин-
большинство из них проводилось при алкогольных ствам урсофалька относятся уменьшение цитолиза и
поражениях печени [60]. Отмечены низкая биодоступ- холестаза, прямое антиапоптозное и иммуномодули-
ность лекарственной формы при приеме внутрь и не- рующее действие. Это единственный эффективный
эффективность при ПБЦ и ПСХ. препарат для лечения ПБЦ (доказательность А) и
Применение гептрала в высоких дозах в III триме- ПСХ (доказательность В). Урсофальк может приме-
стре беременности не вызывает никаких нежелательных няться у детей с момента рождения в виде суспензии;
явлений. Применение препарата в I и II триместрах бере- используется при холестатических заболеваниях пе-
менности и в период грудного вскармливания допусти- чени у беременных (во II—III триместре), практиче-
мо только в тех случаях, когда потенциальная польза для ски лишен побочных эффектов. Эффективность урсо-
матери превышает возможный риск для плода и ребен- фалька подтверждена обширной доказательной базой
ка. Препарат вводят медленно внутривенно капельно по (степень доказательности А—В). Урсофальк является
800 мг в 400 мл физиологического раствора; курс 10— единственным гепатопротектором, рекомендованным
15 дней с переходом на прием внутрь по 400—800 мг FDA к применению у беременных (категория В) [5,
2 раза в сутки между приемами пищи в течение 4 нед. 60]. К недостаткам препарата можно отнести прехо-
Урсодезоксихолевая кислота (УДХК) является ос- дящее послабление стула, что для беременных может
новным препаратом для терапии ПБЦ, ПСХ и других оказаться даже полезным, и отсутствие лекарствен-
заболеваний печени, сопровождающихся синдромом ной формы для парентерального введения, однако в
холестаза, в том числе у беременных [61, 66—70]. соответствии с механизмом действия УДХК следует
УДХК — это гидрофильная липофобная нетоксичная принимать именно внутрь. Во время беременности
третичная желчная кислота (ЖК). На фоне ее приема урсофальк назначают из расчета 10—15 мг/кг в сутки,
существенно снижается энтерогепатическая цирку- разделенные на 2—3 приема (со II триместра), одна-
ляция гидрофобных ЖК, что предупреждает их ток- ко в тех случаях, когда попытка отмены урсофалька
сическое действие на мембраны гепатоцитов и эпите- ухудшает течение заболевания, препарат должен при-
лий желчных протоков. УДХК имеет множество по- меняться на протяжении беременности. Именно на
ложительных свойств: оказывает цитопротективное ранних сроках беременности нервная система плода
(встраивание УДХК в фосфолипидный слой клеточной особенно чувствительна к воздействию токсичных ве-
мембраны), холеретическое (вытеснение из пула гидро- ществ. При нарастании холестаза во время беременно-
фобных токсических ЖКс их выведением в кишечник), сти токсический эффект дают прежде всего гидрофоб-
антихолестатическое (препятствует поступлению ток- ные ЖК и билирубин, уровень которых повышается
сичных ЖК в печень благодаря конкурентному захвату именно при прекращении приема УДХК.
их в подвздошной кишке), регенераторное (стимулиру- При лечении АИЗП в период беременности ис-
ет митоз и регенерацию клеток печени), иммуномоду- пользуют базисные препараты: УДХК, ГКС, а также
14 КЛИНИЧЕСКАЯ МЕДИЦИНА, № 8 , 2015
(по строгим показаниям) цитостатики [51]. К немеди- к зачатию у пациенток с неактивными ВЗК не отличает-
каментозным методам лечения относятся исключение ся от таковой в общей популяции. При высокой актив-
лекарств с гепатотоксическим действием; минимизи- ности болезни Крона и язвенного колита наблюдается
рование физических нагрузок, переутомлений; исклю- вторичная аменорея, развиваются осложнения (свищи,
чение психотравмирующих ситуаций; отказ от физио- абсцессы, спаечный процесс в малом тазу), препятству-
терапевтических процедур; диетические ограничения ющие наступлению беременности. Женщины, страдаю-
с исключением алкоголя, жирных сортов мяса, рыбы, щие ВЗК, составляют группу риска по невынашиванию
птицы, грибов, консервов, копченостей, шоколада. Бла- беременности и гипотрофии плода, однако на детей,
гоприятные условия для функционирования печени родившихся в срок, ВЗК влияния не оказывают [73, 74].
создает постельный режим. Отрицательное влияние ВЗК на течение беременности
При ПБЦ и ПСХ для лечения применяют урсофальк проявляется только в том случае, если беременность
в дозе 15 мг/кг в сутки, разделенные на 2—3 приема; наступает и протекает на фоне высокой активности вос-
энтеросорбенты; препараты кальция в сочетании с ви- палительного процесса в кишечнике. Характер течения
тамином Д3; при наличии инфекционных осложнений ВЗК во время беременности зависит от степени актив-
назначают дезинтоксикационную терапию и антибак- ности воспалительного процесса на момент зачатия.
териальные средства (пенициллины, цефалоспорины). Рецидивы чаще возникают в I триместре беременности,
При АИГ в период беременности абсолютными по- после абортов и родов, что объясняется колебаниями
казаниями для назначения ГКС, по мнению AASLD уровня кортизола. Прерывание беременности при обо-
(Американская ассоциация по изучению заболеваний стрении ВЗК нецелесообразно, поскольку может вызвать
печени) [72], являются уровень АСТ более 10 норм; дальнейшее ухудшение процесса. Поддерживающая те-
уровень АСТ более 5 норм в сочетании с уровнем рапия ВЗК при наступлении беременности должна быть
γ-глобулина более 2 норм; мостовидный или мульти- продолжена, так как повышение активности воспали-
ацинарный некроз. Относительными показаниями к тельного процесса в кишечнике более опасно для плода,
назначению ГКС являются боль в суставах, желтуха, чем возможное воздействие лекарственных препаратов.
повышенная усталость. Неадекватная терапия обострения заболевания или не-
ГКС отнесены FDA к категории С [5]. Для приме- достаточные дозы лекарств более вредны для плода и
нения в период беременности используют низкие и матери, чем продолжение активной фармакотерапии.
средние дозы (доза преднизолона 20— 30 мг/сут). При Основная концепция медикаментозного лечения бе-
назначении более высоких доз, особенно в I триме- ременных с ВЗК: «как можно меньше лекарственных
стре беременности, существует риск гипотрофии пло- препаратов при сохранении контроля над заболевани-
да, замедления его роста, незаращения твердого неба ем» [73, 75, 76].
и верхней губы. Критериями эффективности лечения Сульфасалазин ( отнесен FDA к категории В) [5]
является уровень сывороточных аминотрансфераз и проникает через плацентарный барьер, угнетает транс-
глобулинов. Нужно отметить, что биохимическая ре- порт и метаболизм фолиевой кислоты. Препарат вытес-
миссия предшествует гистологической на 3—6 мес, няет билирубин из его связи с белком, что повышает
поэтому после нормализации биохимических показа- риск возникновения ядерной желтухи плода, однако
телей крови лечение следует продолжать еще в течение установлено, что концентрация билирубина в пуповин-
6—12 мес, после чего дозу ГКС постепенно снижают в ной крови настолько незначительна, что риск развития
течение 6 нед. Использование ГКС в период лактации желтухи ничтожен. Кроме того, многочисленные кли-
также относительно безопасно. Применение будесони- нические наблюдения не выявили побочных эффектов
да при беременности не описано. при применении сульфасалазина у беременных. Назна-
Азатиоприн и 6-мераптопурин ( отнесен FDA к ка- чают его в обычных терапевтических дозах вместе с
тегории D) при беременности используют по строгим фолиевой кислотой [73].
показаниям [5]. Назначают их с крайней осторожно- 5-Аминосалициловая кислота (салофальк) отнесе-
стью и только при наличии высокой активности ау- на FDA к категории В [5] , назначение ее в период бере-
тоиммунного процесса, не контролируемого приемом менности относительно безопасно при дозе 2—3 г/сут.
ГКС. При наступлении беременности цитостатики по Многообразие лекарственных форм 5-аминосалици-
возможности отменяют и заменяют ГКС. Если отмена ловой кислоты позволяет подобрать максимальную
азатиоприна или 6-меркаптопурина обусловливает по- концентрацию в зоне поражения и уменьшить систем-
вышение риска ухудшения течения заболевания, то их ную лекарственную нагрузку [77]. Кроме того, рН-
прием следует продолжить [51]. независимый механизм высвобождения активного ве-
При лечении перекрестного синдрома (overlap щества из гранул, его равномерное распределение по
syndrome) АИГ/ПБЦ (ПСХ) назначают преднизолон в толстой кишке и терапевтическая доза, не превышаю-
дозе 20—30 мг в сутки на протяжении 3—6 мес и урсо- щая 3 г/сут, дают салофальку в гранулах преимущество
фальк по 15 мг/кг в сутки пожизненно. при назначении в период беременности.
Воспалительные заболевания кишечника. ВЗК, ГКС при ВЗК назначают в более высоких дозах
как и другие аутоиммунные заболевания, при беремен- (1— 2 мг/кг), чем при АИЗП, поэтому повышается риск
ности чаще всего протекают благоприятно. Способность возникновения побочных эффектов (незаращение твер-
КЛИНИЧЕСКАЯ МЕДИЦИНА, № 8, 2015 15
дого нёба и верхней губы, гипотрофия плода) [73, 74]. 7. Joshi D., James A., Quagilia А. et al. Liver disease in pregnancy.
Lancet. 2010; 375: 594—605.
Метронидазол (отнесен FDA к категории В) [5, 74] 8. Игнатова Т.М. Заболевания печени у беременных. Медицинский
эффективен при лечении активных форм болезни Кро- вестник Северного Кавказа. 2009; 2: 88—93.
на и безопасен при назначении в низких дозах корот- 9. Карпов О.И., Зайцев А.А. Риск применения лекарств при бере-
менности и лактации: Справочное руководство. СПб.: БХВ —
ким курсом во II и III триместрах беременности. При Санкт-Петербург; 1998.
назначении в I триместре или при длительном приме- 10. Акушерство: Национальное руководство / Под ред. Э.К. Айла-
нении в более высоких дозах повышается риск разви- мазяна, В.А. Кулакова, В.Е. Радзинского, Г.М. Савельевой. М.:
ГЭОТАР-Медиа; 2007.
тия расщелины неба и верхней губы у плода. 11. Куликов А.В. Острые нарушения гемостаза в акушерстве (кро-
Инфликсимаб (ремикейд) отнесен FDA к катего- вотечения и тромбозы): Практическое руководство. Екатерин-
рии В [5, 73, 75]. Достоверных данных об отрицатель- бург; 2007.
12. Бурков С.Г. Гастроэзофагеальная рефлюксная болезнь у женщин
ном влиянии ремикейда на течение беременности нет, в период беременности. Гинекология. 2001; 6 (5): 12—5.
однако, учитывая, что концентрация инфликсимаба в 13. Бурков С.Г. Заболевания органов пищеварения у беременных. М.:
КРОН-ПРЕСС; 1990: 41—61.
крови новорожденного превышает его концентрацию 14. Dean B.B., Crawley J.A., Schmitt C.M., Wong J., Ofman J.J. The
в крови матери, существует потенциальный риск им- burden of illness of gastro-oesophageal reflux disease: impact on
муносупрессии у новорожденного, следствием чего work productivity. Aliment. Pharmacol. Ther. 2003; 17: 1309—17.
15. Salvatore S., Vandenplas Y. Gastro-oesophageal reflux disease and
может стать развитие инфекционных заболеваний. Для motility disorders. Best Pract. Res. Clin. Gastroenterol. 2003; 17:
минимизации побочных эффектов рекомендуется пре- 163—79.
кращение инфузии препарата в начале III триместра 16. Ушкалова Е.А. Лечение гастроэзофагеального рефлюкса у бере-
менных женщин. Гинекология. 2001; 3 (3): 89—90.
беременности. 17. Циммерман Я.С., Вологжанина Л.Г. Гастроэзофагеальная реф-
При планировании беременности у пациенток с люксная болезнь: патогенез, клиника, диагностика и лечение.
Клиническая медицина. 2005; 9: 16—24.
ВЗК необходимо учитывать, что оптимальное время 18. Richter J.E., Kahrilas P.J., Johanson J. et al. Efficacy and safety
для зачатия — период стойкой ремиссии. До зачатия of esomeprazole compared with omeprazole in GERD patients
необходимо проводить определение и коррекцию де- with erosive esophagitis: a randomizet controlled trial. Am. J.
Gastroenterol. 2001; 96: 656—65.
фицита витамина В12, железа, фолиевой кислоты. При 19. Lacroix I., Damase-Michel C., Lapeyre-Mestre M., Montastruc J.L.
наступлении беременности нужно продолжать под- Prescription of drugs during pregnancy in France. Lancet. 2000; 356
держивающую терапию салофальком в гранулах в дозе (18): 1735—6.
20. Richter J.E. gastroesophageal reflux disease during pregnancy.
1,5—2 г/сут. Иммуносупрессоры следует отменить за Gastroenterol. Clin. 2003; 32: 1—5.
3 мес до предполагаемой беременности. 21. Клиническая фармакология / Под ред. Х.П. Кьюмерле, К.М.
Выбор метода родоразрешения определяется аку- Брендел. М.: Медицина, 1987; т. 2.
22. Ching C., Lam S. Antacids: indications and liminations. Drugs.
шерской ситуацией с учетом риска повреждения в ро- 1994; 47: 305—17.
дах тазового дна и анального сфинктера. Пациенткам 23. Magee L.A., Inocencion G., Kambojt R. et al. Safety of first trimester
exposure to histamine H2 blockers: A prospective cohort study. Dig.
с наличием перианальных и ректальных поражений Dis. Sci. 1996; 41: 1145—9.
показано кесарево сечение. Эпизиотомия производится 24. Ruigomez A., Rodrigues L.A.G., Cattaruzzi C. et al. Use of
по строгим показаниям, так как повышает риск возник- cimetidine, omeprazole and ranitidine in pregnant women and
pregnancy outcomes. Am. J. Epidemiol. 1999; 150: 276—481.
новения перианальных осложнений. 25. Brunner G., Meyer H., Athman C. Omeprazole for peptic ulcer
Врач, назначающий фармакотерапию беременной, не- disease in pregnancy. Digestion. 1998; 59: 651—4.
сет персональную ответственность за здоровье как мате- 26. Nikfar S., Abdollahi M., Moretti M.E. et al. Use of proton pump
inhibitors during pregnancy and rates of major malformations. A
ри, так и еще не рожденного ребенка. Для минимизации meta-analysis. Dig. Dis. Sci. 2002; 47(7): 1536—29.
риска отрицательного влияния лекарственных препара- 27. Pasternak B., Hviid A. Use of proton-pump inhibitors in early
тов на развивающийся плод рекомендуется назначать во pregnancy and the risk of birth defects. N. Engl. J. Med. 2010; 363:
2114—23.
время беременности только оригинальные препараты, 28. Kallen B.A. Delivery outcome after the use of acid-suppressing
поскольку именно они, как правило, дают меньше побоч- drugs in early pregnancy with special reference to omeprazole. Br. J.
Obstet. Gynaecol. 1998; 105: 877—81.
ных эффектов. Кроме того, использовать следует только 29. Kallen B.A. Use of omeprazole during pregnancy — no hazard
те препараты, которые абсолютно необходимы! demonstrated in 955 infants exposed during pregnancy. Eur. J.
Obstet. Gynecol. Reprod. Biol. 2001; 96 (1): 63—8.
30. Diav Citrin O., Arnon J., Shechtman S. et al. The safety of proton
Л И Т Е РА Т У РА pump inhibitors in pregnancy: А multicenter prospective controlled
1. Бурков С.Г. Заболевания органов пищеварения у беременных. М.: study. Aliment. Pharmacol. Ther. 2005; 21 (3): 269—75.
КРОН-ПРЕСС; 1996. 31. Еремина Е.Ю., Машарова А.А. Заболевания органов пищевари-
2. Кирющенков А.П. Влияние вредных факторов на плод. М.: Ме- тельной системы у беременных. Саранск; 2009.
дицина; 1978. 32. Scott L.D. Gastrointestinal disease in pregnancy. In: Creasy W.J.,
3. Lewis J.H., Weingold A.B. The committee on FDA-related Resnik R., eds. Material-Fetal Medicine, Principles and Practice.
matters for the American College of Gastroenterology. The use 3rd ed. Philadelphia: Saunders; 2004.
of gastrointestinal drugs during pregnancy and lactation. Am. J. 33. Еремина Е.Ю. Панкреатит у беременных. Практическая меди-
Gastroenterol. 1985; 80 (11): 912—23. цина. Гастроэнтерология. Лекции для врачей общей практики.
4. Еремина Е.Ю. Заболевания органов пищеварительной системы 2012; 3 (12):
у беременных. Гастроэнтерология. СПб. 2011; 4: 2—6. 34. Abu Musa A.A., Usta I.M., Rechdan J.B., Nassar A.H. Recurrent
5. Манадеван Ю., Кейн С. Рекомендации Института Американской hypertriglyceridemia-induced pancreatitis in pregnancy: a mana-
гастроэнтерологической ассоциации по медикаментозному ле- gement dilemma. Pancreas. 2006; 32: 227—8.
чению заболеваний желудочно-кишечного тракта у беременных. 35. Yadav D., Pitchumoni C.S. Issues in hyperlipidemic pancreatitis. J.
Клиническая гастроэнтерология и гепатология (русское изда- Clin. Gastroenterol. 2003; 36: 54—62.
ние). 2008; 1(6): 426—31. 36. Клинические рекомендации. Гастроэнтерология / Под ред.
6. Hay J.E. Liver disease in pregnancy. Hepatology. 2008; 47 (3):
В.Т. Ивашкина. М.: ГЭОТАР-Медиа; 2006.
1067—76.
16 КЛИНИЧЕСКАЯ МЕДИЦИНА, № 8 , 2015
37. Hernandez A., Petrov M.S., Brooks D.C. et al. Acute pancreatitis and Клинические перспективы гастроэнтерологии, гепатологии.
pregnancy: a 10 year single center experience. J. Gastrointest. Surg. 2009; 6: 17—21.
2007; 11: 1623—7. 69. Ивашкин В.Т., Буеверов А.О. Аутоиммунные заболевания пече-
38. Словоходов Е.К. Острый панкреатит при беременности. Новый ни в практике клинициста. М.: М-Вести; 2001.
хирургический архив. 2002; 5 (1): 70. Kano M., Shoda J., Irimura T. et al. Effects of long-term ursodeoxy-
39. Игнатова Т.М. Заболевания печени у беременных: Пособие для cholate administration on expression levels of secretory low-mole-
врачей. М.; 2012. cular-weight phospholipase A2 and mucin genes gallblabladder and
40. Шерлок Ш., Дули Дж. Заболевания печени и желчных путей. biliary composition in patients with multiple cholesterol stones.
Практическое руководство: Пер. с англ. М.; 1999. Hepatology. 1998; 28: 302—13.
41. Игнатова Т.М. Хронические заболевания печени у беременных (ли- 71. Silva R. Bilirubin-induced apoptosis in astrocytes is ursodeoxycholic
тературный обзор). Терапевтический архив. 2002; 7 (10): 55—9. acid. Hepatology. 1998; 28(4): 329A.
42. Pembrey L., Newel M.-L., Tovo P.-A. The EPHN Collaborators. The 72. Ursofalk: Primary Biliary Cirrhosis, Dyspeptic Complains, Chole-
management of HCV infected pregnant woman and their children. J. sterol Gsllstones. Freiburg: Dr. Falk Pharma GmbH; 2005.
Hepatol. 2005; 43: 515—25. 73. Strassburg C.P., Manns M.P. Treatment of autoimmune hepatitis.
43. Игнатова Т.М. Хронический гепатит С и беременность. Клини- Semin. Liver Dis. 2009; 29 (3): 273—85.
ческая гепатология. 2008; 4 (1): 3—9. 74. Методы диагностики и лечения воспалительных заболеваний
44. Gambarin-Gelwan M. Hepatitis B in pregnancy. Clin. Liver Dis. кишечника у женщин репродуктивного возраста: Практическое
2007; 11: 945—63. руководство для врачей / Под ред. Г.А. Григорьевой. М.; 2012.
45. Jonas M.M. Hepatitis B and pregnancy: an underestimated issue. 75. Dignass A. Crohn's disease, ulcerative colititis and pregnancy. In:
Liver Intern. 2009; 29 (Suppl. 1): 133—9. Materials of Falk Symposium. Freiburg; 2002: 51.
46. Lee N.M., Rady C.W. Liver disease in pregnancy. World J. Gastro- 76. Norgard B., Fonager K., Sorensen H.T., Olsen J. Birth outcomes of
enterol. 2009; 15 (8): 897—906. woman with ulcerative colititis: a nationwide Danish cohort study.
47. Poupon R., Chretien Y., Chazouilleres O., Poupon R.E. Pregnancy in Am. J. Gastroenterol. 2000; 95: 3165—70.
woman with ursodeoxycholic acid-treated primary biliary cirrhosis. 77. Beniada A., Benoist G., Maurel M. Inflammatory bowie disease and
J. Hepatol. 2005; 42: 418—9. pregnancy: report of 76 cases and review of the literature. J. Gynecol.
48. Sternlieb I., Wilson S. Disease and pregnancy. Hepatology. 2000; 31: Obstet. Biol. Reprod. 2005; 34: 581—8.
531—2. 78. Циммерман Я.С., Циммерман И.Я., Третьякова Ю.И. Язвенный
49. Приказ Минздравсоцразвития России № 736 от 03.12.2007 г. колит и болезнь Крона. Клиническая медицина. 2013; 11: 27—33;
«Об утверждении перечня медицинских показаний для искус- 12: 9—16.
ственного прерывания беременности». М.; 2007.
50. Еремина Е.Ю. Аутоиммунные заболевания печени и беремен- REFERENCES
ность. Практическая медицина. Акушерство и гинекология.
Лекции для врачей общей практики. 2011; 6 (11): 1. Burkov S.G. Gastrointestinal Diseases in Pregnant Women. Mos-
51. Лейшнер У. Аутоиммунные заболевания печени и перекрестный cow: CROWN PRESS; 1996. (in Russian)
синдром. М.; 2005. 2. Kiryushchenkov A.P. Influence of Harmful Factors on Fetus. Mos-
52. Циммерман Я.С. Аутоиммунный гепатит: патогенез, диагности- cow: Meditsina; 1978. (in Russian)
ка, лечение. Клиническая медицина. 2010; 3: 12—5. 3. Lewis J.H., Weingold A.B. The committee on FDA-related matters
53. Schramm C., Herkel J., Beuers U. et al. Pregnancy in autoimmune for the American College of Gastroenterology. The use of gastroin-
hepatitis: outcome and risk factors. Am. J. Gastroenterol. 2006; 101: testinal drugs during pregnancy and lactation. Am. J. Gastroenterol.
556—60. 1985; 80 (11): 912—23.
54. Heneghan M.A., Noris S.M., O'Grady J.G. et al. Management and 4. Eremina E.Yu. Diseases of gastrointestinal tract in pregnant women.
outcome of pregnancy in autoimmune hepatitis. Gut. 2001; 48: 97— Gastroenterologiya (SPb.). 2011; 4: 2—6. (in Russian)
102. 5. Manadevan Yu., Keyn S. Recommendations of Institute of the Amer-
55. Solomon L., Abrams G., Dinner M., Berman L. Neonatal ican association of gastroenterology about drug treatment of the dis-
abnormalities associated with D-penicillamine treatment during eases of a digestivetract in pregnant women. Klinicheskaya gastroen-
pregnancy. N. Engl. J. Med 1977; 296: 54—5. terologiya i gepatologiya (russkoe izdanie). 2008; 1(6): 426-31. (in
56. Brewer G.J., Johnson V.D., Dick R.D. et al. Treatment of Wilson's Russian)
disease with zinc. XVII: treatment during pregnancy. Hepatology. 6. Hay J.E. Liver disease in pregnancy. Hepatology. 2008; 47 (3):
2000; 31: 364—70. 1067—76.
57. Mahadevan U., Kane S. American gastroenterological association 7. Joshi D., James A., Quagilia А. et al. Liver disease in pregnancy.
Institute Technical Review on the use of gastrointestinal medications Lancet. 2010; 375: 594—605.
in pregnancy. Gastroenterology. 2006; 131: 283—311. 8. Ignatova T.M. Liver diseases in pregnant women. Meditsinskiy vest-
58. Pergam S.A., Wang C.C., Gardella C.M., Sandison T.G., Phipps nik Severnogo Kavkaza. 2009; 2: 88—93. (in Russian)
W.T. Pregnancy complications associated with hepatitis C: data from 9. Karpov O.I., Zaytsev A.A. Risk of Drugs Management atPregnancy
a 2003-2005 Washington state birth cohort. Am. J. Obstet. Gynecol. and Lactation: Reference Guide. St. Petersburg: Bkh — St. Peters-
2008; 199: 38. el—9. burg; 1998. (in Russian)
59. Browej N.H. Hepatitis B therapy in pregnancy. Curr. Hepat. Rep. 10. Obstetrics: National Management / Eds E.K. Aylamazyan, V.A. Ku-
2010; 9: 197—204. lakov, V.E. Radzinskiy, G.M. Savel'yeva. Moscow: GEOTAR-Me-
60. Yogeswaran K., Fung S.K. Chronic hepatitis B in pregnancy: unigue dia; 2007. (in Russian)
challenges and opportunities. Korean J. Hepatol. 2011; 17: 1—8. 11. Kulikov A.V. Acute Disorders of Hemostasis in Obstetrics (Bleed-
61. Кучерявый Ю.А., Морозов С.В. Гепатопротекторы: рацио- ings and Thromboses): Practical Guidance. Yekaterinburg; 2007. (in
нальные аспекты применения: Учебное пособие для врачей. М.; Russian)
2012. 12. Burkov S.G. Gastroezofageal reflux disease in women during preg-
62. Губергриц Н.Б., Лукашевич Г.М., Фоменко П.Г. Гепатопротек- nancy. Ginekologiya. 2001; 6(5): 12—5. (in Russian)
торы: от теории к практике. М.; 2012. 13. Burkov S.G. Diseases of the Digestive System in Pregnant. Moscow:
63. Сравнительная характеристика современных гепатопротекто- CROWN PRESS; 1990: 41—61. (in Russian)
ров. Доктор. 2001; 2: 43—7. 14. Dean B.B., Crawley J.A., Schmitt C.M., Wong J., Ofman J.J. The
64. Подымова С.Д. Внутрипеченочный холестаз: патогенез и ле- burden of illness of gastro-oesophageal reflux disease: impact on
чение адеметионином. Клиническая фармакология и терапия. work productivity. Aliment. Pharmacol. Ther. 2003; 17: 1309—17.
2006; 2: 67—70. 15. Salvatore S., Vandenplas Y. Gastro-oesophageal reflux disease and
65. Яковенко Э.П. Гептрал в лечении внутрипеченочного холеста- motility disorders. Best Pract. Res. Clin. Gastroenterol. 2003; 17:
за. Российский журнал гастроэнтерологии, гепатологии, коло- 163—79.
проктологии. 2002; 1: 84—8. 16. Ushkalova E.A. Treatment of a gastroezofageal reflux disease in
66. Jover R., Pondosa X., Fabra R. et al. S-Adenosyl-L-Methionine pregnant women. Ginekologiya. 2001; 3(3): 89—90. (in Russian)
prevents intracellular glutathione depletion by GSH-depleting drugs in 17. Tsimmerman Ya. S., Vologzanina L.G. Gastroezofageal reflux dis-
rat and human hepatocytes. Drug Invest. 1992; 4(Suppl. 4): 46—53. ease: pathogenesis, clinical, diagnostics and treatment. Kliniches-
67. Khare S., Cerda S., Wali R.K. et al. Ursodeoxycholic acid inhibits kaya meditsina. 2005; 9: 16—24. (in Russian)
Ras mutations, wild-tipe Ras activation, and cyclooxygenase-2 18. Richter J.E., Kahrilas P.J., Johanson J. et al. Efficacy and safety of
expression in colon cancer. Cancer Res. 2003; 63(13): 3517—23. esomeprazole compared with omeprazole in GERD patients with
68. Ивашкин В.Т., Маевская М.В., Федоськина Е.А. Применение erosive esophagitis: a randomizet controlled trial. Am. J. Gastroen-
урсодезоксихолевой кислоты в лечении больных гепатитом С. terol. 2001; 96: 656—65.
КЛИНИЧЕСКАЯ МЕДИЦИНА, № 8, 2015 17
19. Lacroix I., Damase-Michel C., Lapeyre-Mestre M., Montastruc J.L. 50. Eremina E.Yu. Hepar autoimmune diseases and pregnancy. Practice
Prescription of drugs during pregnancy in France. Lancet. 2000; 356 medicine. Obstetrics and gynecology. Lectures for general practitio-
(18): 1735—6. ners. 2011; 6(11): . (in Russian)
20. Richter J.E. gastroesophageal reflux disease during pregnancy. Gas- 51. Leyshner U. Hepar Autoimmune Diseases and a Cross Syndrome.
troenterol. Clin. 2003; 32: 1—5. Moscow; 2005. (in Russian)
21. Clinical Pharmacology / Eds H.P. Kyyumerle, K.M. Brendel. Mos- 52. Tsimmerman Ya.S. Autoimmune hepatitis: pathogenesis, diagnos-
cow: Meditsina; 1987; vol. 2. (in Russian) tics, treatment. Klinicheskaya meditsina. 2010; 3: 12-5. (in Russian)
22. Ching C., Lam S. Antacids: indications and liminations. Drugs. 53. Schramm C., Herkel J., Beuers U. et al. Pregnancy in autoimmune
1994; 47: 305—17. hepatitis: outcome and risk factors. Am. J. Gastroenterol. 2006; 101:
23. Magee L.A., Inocencion G., Kambojt R. et al. Safety of first trimester 556—60.
exposure to histamine H2 blockers: A prospective cohort study. Dig. 54. Heneghan M.A., Noris S.M., O'Grady J.G. et al. Management and out-
Dis. Sci. 1996; 41: 1145—9. come of pregnancy in autoimmune hepatitis. Gut. 2001; 48: 97—102.
24. Ruigomez A., Rodrigues L.A.G., Cattaruzzi C. et al. Use of cimeti- 55. Solomon L., Abrams G., Dinner M., Berman L. Neonatal abnormali-
dine, omeprazole and ranitidine in pregnant women and pregnancy ties associated with D-penicillamine treatment during pregnancy. N.
outcomes. Am. J. Epidemiol. 1999; 150: 276—481. Engl. J. Med. 1977; 296: 54—5.
25. Brunner G., Meyer H., Athman C. Omeprazole for peptic ulcer dis- 56. Brewer G.J., Johnson V.D., Dick R.D. et al. Treatment of Wilson's
ease in pregnancy. Digestion. 1998; 59: 651—4. disease with zinc. XVII: treatment during pregnancy. Hepatology.
26. Nikfar S., Abdollahi M., Moretti M.E. et al. Use of proton pump in- 2000; 31: 364—70.
hibitors during pregnancy and rates of major malformations. A meta- 57. Mahadevan U., Kane S. American gastroenterological association
analysis. Dig. Dis. Sci. 2002; 47(7): 1536—29. Institute Technical Review on the use of gastrointestinal medications
27. Pasternak B., Hviid A. Use of proton-pump inhibitors in early preg- in pregnancy. Gastroenterology. 2006; 131: 283—311.
nancy and the risk of birth defects. N. Engl. J. Med. 2010; 363: 58. Pergam S.A., Wang C.C., Gardella C.M., Sandison T.G., Phipps
2114—23. W.T. Pregnancy complications associated with hepatitis C: data from
28. Kallen B.A. Delivery outcome after the use of acid-suppressing a 2003-2005 Washington state birth cohort. Am. J. Obstet. Gynecol.
drugs in early pregnancy with special reference to omeprazole. Br. J. 2008; 199: 38. el—9.
Obstet. Gynaecol. 1998; 105: 877—81. 59. Browej N.H. Hepatitis B therapy in pregnancy. Curr. Hepat. Rep.
29. Kallen B.A. Use of omeprazole during pregnancy — no hazard dem- 2010; 9: 197—204.
onstrated in 955 infants exposed during pregnancy. Eur. J. Obstet. 60. Yogeswaran K., Fung S.K. Chronic hepatitis B in pregnancy: unigue
Gynecol. Reprod. Biol. 2001; 96 (1): 63—8. challenges and opportunities. Korean J. Hepatol. 2011; 17: 1—8.
30. Diav Citrin O., Arnon J., Shechtman S. et al. The safety of proton 61. Kycheryavyy Yu.A., Morozov S.V. Hepatoprotectors: Rational As-
pump inhibitors in pregnancy: А multicenter prospective controlled pects of Application: Manual for Doctors. Moscow; 2012. (in Russian)
study. Aliment. Pharmacol. Ther. 2005; 21 (3): 269—75. 62. Gubergrits N.B., Lukashevich G.M., Fomenko P.G. Hepatoprotek-
31. Eremina E.Yu., Masharova A.A. Diseases of Gastrointestinal Tract tors: from the Theory to Practice. Moscow; 2012. (in Russian)
in Pregnant Women. Saransk; 2009. (in Russian) 63. Comparative characteristic of modern hepatoprotektors. Doktor.
32. Scott L.D. Gastrointestinal disease in Pregnancy. In: Creasy W.J., 2001; 2: 43-7. (in Russian)
Resnik R., eds. Material-Fetal Medicine, Principles and Practice. 64. Podymova S.D. Interahepatic cholestasis: pathogenesis and ademe-
3rd ed. Philadelphia: Saunders; 2004. tionin treatment. Klinicheskaya farmakologiya i terapiya. 2006; 2:
33. Eremina E.Yu. Pankreatitis in pregnant women. Practical medicine. 67—70. (in Russian)
Gastroenterology. Lectures for general practitioners. 2012; 3(12): . 65. Yakovenko E.P. Geptral in treatment of an intra hepatic cholestas.
(in Russian) Rossiyskiy zhurnal gastroenterologii, gepatologii, koloproktologii.
34. Abu Musa A.A., Usta I.M., Rechdan J.B., Nassar A.H. Recurrent 2002; 1: 84-8. (in Russian)
hypertriglyceridemia-induced pancreatitis in pregnancy: a manage- 66. Jover R., Pondosa X., Fabra R. et al. S-Adenosyl-L-Methionine pre-
ment dilemma. Pancreas. 2006; 32: 227—8. vents intracellular glutathione depletion by GSH-depleting drugs in
35. Yadav D., Pitchumoni C.S. Issues in hyperlipidemic pancreatitis. J. rat and human hepatocytes. Drug Invest. 1992; 4(Suppl. 4): 46—53.
Clin. Gastroenterol. 2003; 36: 54—62. 67. Khare S., Cerda S., Wali R.K. et al. Ursodeoxycholic acid inhibits
36. Clinical Recommendations: Gastroenterology / Ed. V.T. Ivashkin. Ras mutations, wild-tipe Ras activation, and cyclooxygenase-2 ex-
Moscow: GEOTAR-Media; 2006. (in Russian) pression in colon cancer. Cancer Res. 2003; 63(13): 3517—23.
37. Hernandez A., Petrov M.S., Brooks D.C. et al. Acute pancreatitis and 68. Ivashkin V.T., Mayevskaya M.V., Fedoskina E.A. Ursodezoksikholevy
pregnancy: a 10 year single center experience. J. Gastrointest. Surg. acid in treatment of patients with hepatitis C. Klinicheskie perspektivy
2007; 11: 1623-7. gastroenterologii, gepatologii. 2009; 6: 17—21. (in Russian)
38. Slovokhodov E.K. Acute pancreatitis in pregnancy. Novyy khirur- 69. Ivashkin V.T., Buyeverov A.O. Autoimmune Diseases of a Liver in
gicheskiy arkhiv. 2002; 5(1): . (in Russian) Practice of the Clinical Physician. Moscow: M-News; 2001. (in
39. Ignatova T.M. Liver Diseases in Pregnant Women: A Grant for Doc- Russian)
tors. Moscow; 2012. (in Russian) 70. Kano M., Shoda J., Irimura T. et al. Effects of long-term ursode-
40. Sherlock Sh., Duly Dxhy. Diseases of Liver and Bilious Tracts: oxycholate administration on expression levels of secretory low-
Practical Guidance: Transl. from Engl. Moscow; 1999. (in Russian) molecular-weight phospholipase A2 and mucin genes gallblabladder
41. Ignatova T.M. Chronic diseases of a liver in pregnant women (the and biliary composition in patients with multiple cholesterol stones.
literary review). Terapevticheskiy arkhiv. 2002; 7(10): 55-9. (in Rus- Hepatology. 1998; 28: 302—13.
sian) 71. Silva R. Bilirubin-induced apoptosis in astrocytes is ursodeoxycholic
42. Pembrey L., Newel M.-L., Tovo P.-A. The EPHN Collaborators. The acid. Hepatology. 1998; 28(4): 329A.
management of HCV infected pregnant woman and their children. 72. Ursofalk: Primary Biliary Cirrhosis, Dyspeptic Complains, Choles-
J. Hepatol. 2005; 43: 515—25. terol Gsllstones. Freiburg: Dr. Falk Pharma GmbH; 2005.
43. Ignatova T.M. Chronic hepatitis C and pregnancy. Klinicheskaya ge- 73. Strassburg C.P., Manns M.P. Treatment of autoimmune hepatitis. Se-
patologiya. 2008; 4(1): 3—9. (in Russian) min. Liver Dis. 2009; 29 (3): 273—85.
44. Gambarin-Gelwan M. Hepatitis B in pregnancy. Clin. Liver Dis. 74. Methods of Diagnostics and Treatment of Inflammatory Bowel Dis-
2007; 11: 945—63. eases in Reproductive Age Women: Practical Guidance for Doctors /
45. Jonas M.M. Hepatitis B and pregnancy: an underestimated issue. Ed. G.A. Grigor'eva. Moscow; 2012. (in Russian)
Liver Intern. 2009; 29 (Suppl. 1): 133—9. 75. Dignass A. Crohn's disease, ulcerative colititis and pregnancy. In:
46. Lee N.M., Rady C.W. Liver disease in pregnancy. World J. Gastroen- Materials of Falk Symposium. Freiburg; 2002: 51.
terol. 2009; 15 (8): 897—906. 76. Norgard B., Fonager K., Sorensen H.T., Olsen J. Birth outcomes of
47. Poupon R., Chretien Y., Chazouilleres O., Poupon R.E. Pregnancy in woman with ulcerative colititis: a nationwide Danish cohort study.
woman with ursodeoxycholic acid-treated primary biliary cirrhosis. Am. J. Gastroenterol. 2000; 95: 3165—70.
J. Hepatol. 2005; 42: 418—9. 77. Beniada A., Benoist G., Maurel M. Inflammatory bowie disease and
48. Sternlieb I., Wilson S. Disease and pregnancy. Hepatology. 2000; 31: pregnancy: report of 76 cases and review of the literature. J. Gynecol.
531—2. Obstet. Biol. Reprod. 2005; 34: 581—8.
49. The Order of the Ministry of Health and Social Development of Rus- 78. Tsimmerman Ya.S., Tsimmerman I.Ya., Tret'yakova Yu.I. Ulcerative
sian Federation No. 736 of 03.12.2007. "Approval the List of Medi- colitis and Crone disease. Klinicheskaya meditsina. 2013; 11: 27—
cal Indications for Artificial Interruption of Pregnancy. Moscow; 33; 12: 9—16. (in Russian)
2007. (in Russian) Поступила (received) 20.12.14
18 КЛИНИЧЕСКАЯ МЕДИЦИНА, № 8 , 2015
Вам также может понравиться
- Умное материнство. Беременность и роды без домыслов и мифов. Советы мамы-акушераОт EverandУмное материнство. Беременность и роды без домыслов и мифов. Советы мамы-акушераОценок пока нет
- LekterДокумент33 страницыLekterNadya SkimbatorОценок пока нет
- Pregnancy - American Dental AssociationДокумент19 страницPregnancy - American Dental AssociationDan ȚărușОценок пока нет
- IndinolДокумент6 страницIndinolАнна ВарданянОценок пока нет
- 29 TretyakovaДокумент2 страницы29 TretyakovaАлександра ШинкаренкоОценок пока нет
- Struktura Atrezii Zheludochno Kishechnogo Trakta U Novorozhdennyh I Ih Vyzhivaemost Pri Dannoy PatologiiДокумент7 страницStruktura Atrezii Zheludochno Kishechnogo Trakta U Novorozhdennyh I Ih Vyzhivaemost Pri Dannoy PatologiisovrukaiОценок пока нет
- Kliniko Immunologicheskie Vzaimosvyazi Pri Priv Chnom Nev Nashivanii Beremennosti I Metod Ih Korrektsii ObzorДокумент6 страницKliniko Immunologicheskie Vzaimosvyazi Pri Priv Chnom Nev Nashivanii Beremennosti I Metod Ih Korrektsii ObzorAndrei JentimirОценок пока нет
- Современные Взгляды На Патогенетические Аспекты Синдрома Поликистозных Яичников У Женщин Репродуктивного Возраста. Современные Подходы К Выбору Диагностики И ЛеченияДокумент8 страницСовременные Взгляды На Патогенетические Аспекты Синдрома Поликистозных Яичников У Женщин Репродуктивного Возраста. Современные Подходы К Выбору Диагностики И ЛеченияCentral Asian StudiesОценок пока нет
- Ageeva T. Vse o DetyahДокумент474 страницыAgeeva T. Vse o DetyahСофья Генсон50% (2)
- Sovremennye Podhody K Diagnostike Medikamentoznoy Terapii I Profilaktike Akusherskih Oslozhneniy U Zhenschin S TrombofilieyДокумент9 страницSovremennye Podhody K Diagnostike Medikamentoznoy Terapii I Profilaktike Akusherskih Oslozhneniy U Zhenschin S TrombofilieymarinaОценок пока нет
- Цой ВикторияДокумент5 страницЦой ВикторияabdulloshoshoОценок пока нет
- Вмешательства В Перинатальный Период Для Предотвращения Мертворождения, Утраты Плода И Перинатальной СмертностиДокумент8 страницВмешательства В Перинатальный Период Для Предотвращения Мертворождения, Утраты Плода И Перинатальной СмертностиCentral Asian StudiesОценок пока нет
- Роль Патологии Эндометрия При Репродуктивных Потерях В Ранних Сроках БеременностиДокумент3 страницыРоль Патологии Эндометрия При Репродуктивных Потерях В Ранних Сроках БеременностиCentral Asian StudiesОценок пока нет
- 673122Документ32 страницы673122Алена ЧолакОценок пока нет
- АбортыДокумент40 страницАбортыАнастасия ПаскалОценок пока нет
- Novie Shemi Naznachenija Gormonalnih KontratseptivovДокумент7 страницNovie Shemi Naznachenija Gormonalnih KontratseptivovAnna JuniedОценок пока нет
- акушерские кровотеченияДокумент77 страницакушерские кровотеченияОльга РапицкаяОценок пока нет
- Current Approaches To Treatment of AntiphospholipiДокумент6 страницCurrent Approaches To Treatment of Antiphospholipigheorghegaina707Оценок пока нет
- Роль Урогенитальных Инфекций Беременных Женщин С Отхождением Околоплодных ВодДокумент8 страницРоль Урогенитальных Инфекций Беременных Женщин С Отхождением Околоплодных ВодCentral Asian StudiesОценок пока нет
- 2 Met Rekom RusДокумент78 страниц2 Met Rekom RusSergiu MaliiОценок пока нет
- ГУС синдромДокумент18 страницГУС синдромdamir2001164Оценок пока нет
- Rep 2012 03 088Документ6 страницRep 2012 03 088zabrodinayuliyaОценок пока нет
- Rep 2012 02 098Документ6 страницRep 2012 02 098shetinina.lyubaОценок пока нет
- Капрош СтатьяДокумент23 страницыКапрош СтатьяCristinaCaprosОценок пока нет
- 2442 2735 1 PBДокумент5 страниц2442 2735 1 PBBeqa DatebashviliОценок пока нет
- Inflammatory Disease of The Womans Reproductive SyДокумент7 страницInflammatory Disease of The Womans Reproductive SygfhfОценок пока нет
- Istoriya Rodov 2019Документ112 страницIstoriya Rodov 2019Djgernaut DotinОценок пока нет
- Внутриутробная Задержка Роста ПлодаДокумент30 страницВнутриутробная Задержка Роста ПлодаOzhen0% (1)
- UntitledДокумент315 страницUntitledTriple AОценок пока нет
- Zhenskoe Zdorove KnigiДокумент5 страницZhenskoe Zdorove KnigiЖансая ҚұрмантайОценок пока нет
- Klin Derm 2014 05 011Документ7 страницKlin Derm 2014 05 011vladimir.peretyaginОценок пока нет
- ИстмикоДокумент17 страницИстмикоАнатолій БородаОценок пока нет
- Tumor Growth GM Ru 2023Документ21 страницаTumor Growth GM Ru 2023kabulkabulovich5Оценок пока нет
- Dietoprofilaktika Pischevoy Allergii U Grudnyh DeteyДокумент6 страницDietoprofilaktika Pischevoy Allergii U Grudnyh DeteyЛилиана Туровец-ГрицайОценок пока нет
- Sposoby Povysheniya Zhizneustoychivosti Zhivotnyh V Rannem Postnatalnom OntogenezeДокумент6 страницSposoby Povysheniya Zhizneustoychivosti Zhivotnyh V Rannem Postnatalnom Ontogenezesmirnov.capital01Оценок пока нет
- Иммуногистохимические И Патоморфологические Особенности Эндометрия При Привычном Невынашивании Беременности В Ранних СрокахДокумент13 страницИммуногистохимические И Патоморфологические Особенности Эндометрия При Привычном Невынашивании Беременности В Ранних СрокахCentral Asian StudiesОценок пока нет
- 2015 Med Genetika Dlya Studentov VSOДокумент87 страниц2015 Med Genetika Dlya Studentov VSOzalilovaumutajОценок пока нет
- Celiac Disease Russian 2005Документ18 страницCeliac Disease Russian 2005doctor ritaОценок пока нет
- Specifics of Allelic Polymorphism of Genes AssociaДокумент6 страницSpecifics of Allelic Polymorphism of Genes Associabreastcancer.globaleventsОценок пока нет
- Преждевремменый Разрыв Плотных ОболочекДокумент26 страницПреждевремменый Разрыв Плотных ОболочекNurgazy BatyrovОценок пока нет
- Мажитаев Нурмат 38грДокумент10 страницМажитаев Нурмат 38грnurjanovaseilОценок пока нет
- EndometriozДокумент14 страницEndometriozhfjggyОценок пока нет
- Развитие Плода и Витамины-1Документ11 страницРазвитие Плода и Витамины-1Михаил МиряевОценок пока нет
- Влияние Аборта На Здоровье ЖДокумент16 страницВлияние Аборта На Здоровье Жproskurinaanna6Оценок пока нет
- Elibrary 45646508 42037179Документ10 страницElibrary 45646508 42037179jetmaxus.turkey2023Оценок пока нет
- Состояние Тромбоцитарного Гемостаза При Беременности: Признаки Нормы И ПатологииДокумент4 страницыСостояние Тромбоцитарного Гемостаза При Беременности: Признаки Нормы И ПатологииCentral Asian StudiesОценок пока нет
- методичка сепсисДокумент109 страницметодичка сепсисInna LiashenkoОценок пока нет
- Реферат на тему "Профилактика онкологических заболеваний "Документ10 страницРеферат на тему "Профилактика онкологических заболеваний "ДарьяОценок пока нет
- Протокол неразвивающаяся беременностьДокумент16 страницПротокол неразвивающаяся беременностьОльга НестероваОценок пока нет
- Динамика Дисфункций Желудочно-Кишечного Тракта В Аспекте ФизиологииДокумент5 страницДинамика Дисфункций Желудочно-Кишечного Тракта В Аспекте ФизиологииCentral Asian StudiesОценок пока нет
- Гепатоз беременныхДокумент15 страницГепатоз беременныхИрина МисанОценок пока нет
- Характеристика Беременности И Родов У Женщин При Сочетании Антифосфолипидного Синдрома И Коронавирусной ИнфекцииДокумент6 страницХарактеристика Беременности И Родов У Женщин При Сочетании Антифосфолипидного Синдрома И Коронавирусной ИнфекцииCentral Asian StudiesОценок пока нет
- Билет 17Документ6 страницБилет 17gulbitzkyОценок пока нет
- Срс гинекологияДокумент16 страницСрс гинекологияRyskul AnarbekovaОценок пока нет
- вторичный СД эндокринопатииДокумент4 страницывторичный СД эндокринопатииmichaelchigrinskiiОценок пока нет
- Беременность и роды у несовершеннолетнихДокумент6 страницБеременность и роды у несовершеннолетнихRomanОценок пока нет
- Недостаточность питания у детей раннего возраста. Принципы нутритивной поддержки инструкцияДокумент25 страницНедостаточность питания у детей раннего возраста. Принципы нутритивной поддержки инструкцияreznik.anna4Оценок пока нет
- Папилломавирусная Инфекция Урогенитального Тракта у ЖенщинДокумент60 страницПапилломавирусная Инфекция Урогенитального Тракта у ЖенщинLolaR RiОценок пока нет
- Клинико ситуационные задачи при беременностиДокумент52 страницыКлинико ситуационные задачи при беременностиAigerimОценок пока нет
- МРП для врачей 2Документ53 страницыМРП для врачей 2Ольга НестероваОценок пока нет
- Жизнь без боли в спине. Лечение остеохондроза, межпозвонковой грыжи, сколиоза, остеопороза без операции (Zhizn' bez boli v spine. Lechenie osteohondroza, mezhpozvonkovoj gryzhi, skolioza, osteoporoza bez operacii)От EverandЖизнь без боли в спине. Лечение остеохондроза, межпозвонковой грыжи, сколиоза, остеопороза без операции (Zhizn' bez boli v spine. Lechenie osteohondroza, mezhpozvonkovoj gryzhi, skolioza, osteoporoza bez operacii)Оценок пока нет
- Большой универсальный справочник лекарственных препаратов. Более 5000 современных средств и аналогов (Bol'shoj universal'nyj spravochnik lekarstvennyh preparatov. Bolee 5000 sovremennyh sredstv i analogov)От EverandБольшой универсальный справочник лекарственных препаратов. Более 5000 современных средств и аналогов (Bol'shoj universal'nyj spravochnik lekarstvennyh preparatov. Bolee 5000 sovremennyh sredstv i analogov)Оценок пока нет
- Танатотерапия: теоретические основы и практическое применениеОт EverandТанатотерапия: теоретические основы и практическое применениеОценок пока нет
- Природные целители от 1000 болезней (Prirodnye celiteli ot 1000 boleznej)От EverandПриродные целители от 1000 болезней (Prirodnye celiteli ot 1000 boleznej)Оценок пока нет
- Хорошее зрение. Как избавиться от близорукости, дальнозоркости, глаукомы, катаракты (Horoshee zrenie. Kak izbavit'sja ot blizorukosti, dal'nozorkosti, glaukomy, katarakty)От EverandХорошее зрение. Как избавиться от близорукости, дальнозоркости, глаукомы, катаракты (Horoshee zrenie. Kak izbavit'sja ot blizorukosti, dal'nozorkosti, glaukomy, katarakty)Оценок пока нет
- Бабушкин лечебник. Миллион исцеляющих секретов и рецептов народных знахарей (Babushkin lechebnik. Million isceljajushhih sekretov i receptov narodnyh znaharej)От EverandБабушкин лечебник. Миллион исцеляющих секретов и рецептов народных знахарей (Babushkin lechebnik. Million isceljajushhih sekretov i receptov narodnyh znaharej)Оценок пока нет
- Психология, депрессия и расстройства настроения: Понимание основных механизмов депрессии и связанных с ней нарушенийОт EverandПсихология, депрессия и расстройства настроения: Понимание основных механизмов депрессии и связанных с ней нарушенийОценок пока нет
- Лечебник потомственного деревенского знахаря. Исцеление народными методами любых хворей (Lechebnik potomstvennogo derevenskogo znaharja. Iscelenie narodnymi metodami ljubyh hvorej)От EverandЛечебник потомственного деревенского знахаря. Исцеление народными методами любых хворей (Lechebnik potomstvennogo derevenskogo znaharja. Iscelenie narodnymi metodami ljubyh hvorej)Оценок пока нет
- Медицинская и судебная психология. Курс лекций : Учебное пособиеОт EverandМедицинская и судебная психология. Курс лекций : Учебное пособиеТ. Б. ДмитриеваОценок пока нет
- Чистка суставов, крови и сосудов (Chistka sustavov, krovi i sosudov)От EverandЧистка суставов, крови и сосудов (Chistka sustavov, krovi i sosudov)Рейтинг: 5 из 5 звезд5/5 (1)
- Курс леченуя Бройсса: Советы по предупреждению и естественному излечению от различных (кажущихся неизлечимых) заболеваний. Из личного опыта моей многолетн...От EverandКурс леченуя Бройсса: Советы по предупреждению и естественному излечению от различных (кажущихся неизлечимых) заболеваний. Из личного опыта моей многолетн...Рейтинг: 5 из 5 звезд5/5 (1)
- Полный медицинский справочник. Диагностика. Симптоматика.Лечение (Polnyj medicinskij spravochnik. Diagnostika. Simptomatika.Lechenie)От EverandПолный медицинский справочник. Диагностика. Симптоматика.Лечение (Polnyj medicinskij spravochnik. Diagnostika. Simptomatika.Lechenie)Оценок пока нет
- Классик московской психиатрии В.П.Сербский: К 150-летию со дня рожденияОт EverandКлассик московской психиатрии В.П.Сербский: К 150-летию со дня рожденияОценок пока нет
- Диагностика заболеваний. Медицинский справочник (Diagnostika zabolevanij. Medicinskij spravochnik)От EverandДиагностика заболеваний. Медицинский справочник (Diagnostika zabolevanij. Medicinskij spravochnik)Рейтинг: 5 из 5 звезд5/5 (1)
- 120 / 80. Как привести давление в норму без таблеток (120 / 80. Kak privesti davlenie v normu bez tabletok)От Everand120 / 80. Как привести давление в норму без таблеток (120 / 80. Kak privesti davlenie v normu bez tabletok)Оценок пока нет
- Как снять очки за 10 занятий без операции (Kak snjat' ochki za 10 zanjatij bez operacii)От EverandКак снять очки за 10 занятий без операции (Kak snjat' ochki za 10 zanjatij bez operacii)Оценок пока нет