Академический Документы
Профессиональный Документы
Культура Документы
Аминокислоты
Загружено:
Genosse Kommissar0 оценок0% нашли этот документ полезным (0 голосов)
6 просмотров14 страницАвторское право
© © All Rights Reserved
Доступные форматы
PPTX, PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате PPTX, PDF, TXT или читайте онлайн в Scribd
0 оценок0% нашли этот документ полезным (0 голосов)
6 просмотров14 страницАминокислоты
Загружено:
Genosse KommissarАвторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате PPTX, PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 14
Аминокислоты
Подготовил: студент ЕН-БХБ-512 Омариев
Артём
Глицин
• Глицин (аминоуксусная кислота,
аминоэтановая кислота сокр.:
«G», химическая
формула — C2H5NO2) —
простейшая органическая алифатичес
кая аминокислота, относящаяся к
классу карбоновых кислот.
Физико-химические
свойства
• Глицин — твёрдое вещество,
сладковатого вкуса. Неэлектролит.
Единственная протеиногенная
аминокислота, не
имеющая оптических изомеров.
• Глицин, как кислота, с ионами
металлов образует сложные соли
(глицинаты или хелаты): глицинат
натрия, глицина
железа, глицина меди, глицинат
цинка, глицинат марганца и др.
Получение
• Глицин можно получить в ходе хлорирования карбоновых кислот
и дальнейшего взаимодействия с аммиаком:
Биохимия
• Глицин входит в состав многих белков и биологически активных
соединений. Из глицина в живых клетках
синтезируются порфирины и пуриновые основания.
• Глицин также является нейромедиаторной аминокислотой,
проявляющей двоякое действие. Глициновые рецепторы имеются
во многих участках головного мозга и спинного мозга. Связываясь
с рецепторами (кодируемые генами GLRA1, GLRA2, GLRA3 и
GLRB), глицин вызывает «тормозящее» воздействие на нейроны,
уменьшает выделение из нейронов «возбуждающих»
аминокислот, таких как глутаминовая кислота, и повышает
выделение ГАМК. Также глицин связывается со специфическими
участками NMDA-рецепторов и, таким образом, способствует
передаче сигнала от возбуждающих нейротрансмиттеров
глутамата и аспартата.
Применение
Пролин
• Пролин (пирролидин-α-карбоновая
кислота) — гетероциклическая амино
кислота, в которую атом азота входит
в составе вторичного, а не
первичного, амина (в связи с чем
пролин правильнее
называть иминокислотой). Существует
в двух оптически
изомерных формах — L и D, а также в
виде рацемата.
Физико-химические свойства
• Представляет собой бесцветные, легко растворимые в воде
кристаллы, плавящиеся при температуре около 220 °C. Также
хорошо растворим в этаноле, хуже — в ацетоне и бензоле,
нерастворим в диэтиловом эфире.
• В организме пролин синтезируется из глутаминовой кислоты.
• Пролин, как и гидроксипролин, в отличие от других аминокислот,
не образует с нингидрином пурпура Руэмана, а дает жёлтое
окрашивание.
• В составе коллагена пролин при участии аскорбиновой кислоты
окисляется в гидроксипролин. Чередующиеся остатки молекулы
пролина и гидроксипролина способствуют созданию стабильной
трёхспиральной структуры коллагена, придающей молекуле
прочность.
Лабораторный
синтез
• Рацемическая смесь L- и D-пролина
может быть получена из
диэтилового эфира малоновой
кислоты и акрилонитрила.
Биологическая роль
и применение
Лизин
• Лизин (2,6-диаминогексановая
кислота, лат. lysin) — алифатическая
аминокислота с выраженными
свойствами основания. Как и другие
алифатические аминокислоты, лизин в
организме человека не синтезируется
и является незаменимой
аминокислотой.
• Химическая формула: C6H14N2O2.
• В ДНК кодируется
последовательностями AAA и AAG.
• Входит в состав белков.
Физико-химические
свойства
• Лизин кристаллизуется в виде бесцветных игл или
пластинок и плавится с разложением при температуре
2240С. Хорошо растворим в воде, в кислотах и основаниях,
трудно растворим в спирте и нерастворим в эфире.
• Аминокислоты проявляют свойства оснований за счет
аминогрупп и свойства кислот за счет карбоксильных
групп, то есть являются амфотерными соединениями.
Молекулы аминокислот в растворах существуют в виде
внутренних солей, которые образуются за счет переноса
протона от карбоксила к аминогруппе.
• Благодаря наличию карбоксильной и аминных групп, лизин
может участвовать в специфических химических реакциях.
Он образует соли, сложные эфиры, гидразиды, азиды,
тиоэфиры, галогенатгидриды. Например, с соляной
кислотой лизин образует гидрохлориды.
• Жизненно важными для человека являются реакции
образования пептидов и белков с участием лизина.
Биохимия и
получение
Применение
Вам также может понравиться
- АминокислотыДокумент13 страницАминокислотыmatushenko.n14Оценок пока нет
- Технология Витамина В6 и Витамина СДокумент8 страницТехнология Витамина В6 и Витамина СНастя КуликоваОценок пока нет
- Аминокислота и Ее Биологическая ЦенностьДокумент12 страницАминокислота и Ее Биологическая ЦенностьDiana KadyrОценок пока нет
- Лекция Технология и Свойства Витаминов А и РРДокумент10 страницЛекция Технология и Свойства Витаминов А и РРНастя КуликоваОценок пока нет
- 23 Первоначальные понятия об органических веществах как о соединениях углерода PDFДокумент30 страниц23 Первоначальные понятия об органических веществах как о соединениях углерода PDFДаниил ПалиховОценок пока нет
- АминокислотыДокумент6 страницАминокислотыDiva MokhammadОценок пока нет
- лейцинДокумент2 страницылейцинВладислав ОрловОценок пока нет
- Суперметода по биохимииДокумент368 страницСуперметода по биохимииimantaeva0577Оценок пока нет
- Slozhnye Efiry I Zhiry Stepenin RuДокумент9 страницSlozhnye Efiry I Zhiry Stepenin Rujamosa2007Оценок пока нет
- Сложные Эфиры и ЖирыДокумент14 страницСложные Эфиры и ЖирыАян КалиевОценок пока нет
- Витамины текстДокумент5 страницВитамины текстKarim DahduhОценок пока нет
- Лек - 8 - Неделя Карбоновые кислотыДокумент4 страницыЛек - 8 - Неделя Карбоновые кислотыarinaОценок пока нет
- Носители для иммобилизации ферментовДокумент28 страницНосители для иммобилизации ферментовkost9n12Оценок пока нет
- Кислородсодержащие органические соединенияДокумент24 страницыКислородсодержащие органические соединенияkillerutegenovОценок пока нет
- Lecture - 3Документ18 страницLecture - 3LadaОценок пока нет
- Spirty Stepenin RuДокумент8 страницSpirty Stepenin Ruyoung pipОценок пока нет
- Какой Углевод Не Растворяется в Воде и Не Имеет Сладкого Вкуса - Поиск в GoogleДокумент1 страницаКакой Углевод Не Растворяется в Воде и Не Имеет Сладкого Вкуса - Поиск в GoogleНечипоренко КоляОценок пока нет
- Спирты (часть - 1)Документ34 страницыСпирты (часть - 1)vassiliy.kachalov.jrОценок пока нет
- ЭфирыДокумент4 страницыЭфирыuleftkidnqweyОценок пока нет
- Метаболизм жиров полная версия - 1655111534Документ36 страницМетаболизм жиров полная версия - 1655111534ElenaОценок пока нет
- 136 02Документ58 страниц136 02Knizhonki KnizhonkiОценок пока нет
- гликозидиДокумент43 страницыгликозидиАнжелика ДенежкинаОценок пока нет
- 311191Документ35 страниц311191Erzhigit ZhorakhanovОценок пока нет
- 1.4. Metabolismul Lipidelor Ru 2021-2022 StudДокумент206 страниц1.4. Metabolismul Lipidelor Ru 2021-2022 StudgdominatingОценок пока нет
- БиологияДокумент25 страницБиологияvladneradailОценок пока нет
- Karbonovye Kisloty Stepenin RuДокумент12 страницKarbonovye Kisloty Stepenin Ruyoung pipОценок пока нет
- XI - Chimia (A. 2020 in Limba Rusa) - 70-75Документ6 страницXI - Chimia (A. 2020 in Limba Rusa) - 70-75Diana GuzunОценок пока нет
- АминокислотыДокумент18 страницАминокислотыМария СкопченкоОценок пока нет
- Aminokisloty Struktura I Funktsia 2Документ57 страницAminokisloty Struktura I Funktsia 2Александр ФеоктистовОценок пока нет
- БелкиДокумент5 страницБелкиmatushenko.n14Оценок пока нет
- SFKH 2020-1 Public AlcoДокумент503 страницыSFKH 2020-1 Public AlcoСофияОценок пока нет
- фенолыДокумент56 страницфенолыbumbasterОценок пока нет
- Kompleksnaya Otsenka Kachestva Alyumoi Zhelezosoderzhaschih Reagentov Dlya Ochistki VodyДокумент8 страницKompleksnaya Otsenka Kachestva Alyumoi Zhelezosoderzhaschih Reagentov Dlya Ochistki Vodynosser2017Оценок пока нет
- Крок 1.БіохіміяДокумент28 страницКрок 1.БіохіміяevolokhhОценок пока нет
- Mahmoud ChemistryДокумент292 страницыMahmoud ChemistryBilalОценок пока нет
- Karbonilnye Soedinenia Stepenin RuДокумент13 страницKarbonilnye Soedinenia Stepenin Ruyoung pipОценок пока нет
- фенолыДокумент6 страницфенолыbumbasterОценок пока нет
- АльдегидыДокумент7 страницАльдегидыKarim DahduhОценок пока нет
- миДокумент10 страницмиcosmviieОценок пока нет
- 1. Лекция Углеводы ЛипидыДокумент4 страницы1. Лекция Углеводы ЛипидыДмитрий КондратьевОценок пока нет
- ВитаминыДокумент20 страницВитаминыVlad FilariusОценок пока нет
- Химия 9 класс. Хлоровод кислота ПрезентацияДокумент10 страницХимия 9 класс. Хлоровод кислота ПрезентацияlofisoulmusicОценок пока нет
- Спирты (часть - 2)Документ38 страницСпирты (часть - 2)vassiliy.kachalov.jrОценок пока нет
- Uglevodnyi 774 ObmenДокумент139 страницUglevodnyi 774 ObmenАлександр ФеоктистовОценок пока нет
- Aminy Anilin Stepenin RuДокумент8 страницAminy Anilin Stepenin Rujamosa2007Оценок пока нет
- УглеводыДокумент28 страницУглеводыGutОценок пока нет
- Чичибабин редакт.Документ18 страницЧичибабин редакт.Сергей ВладимировОценок пока нет
- Биохимия соединительной тканиДокумент54 страницыБиохимия соединительной тканиНаталья ГороховаОценок пока нет
- AminoaciziДокумент24 страницыAminoaciziMorteanu EleonoraОценок пока нет
- Классификация аминокислот на основе их предшественников в метаболизмеДокумент17 страницКлассификация аминокислот на основе их предшественников в метаболизмеElenaОценок пока нет
- Альдегиды и Кетоны.базаpptДокумент17 страницАльдегиды и Кетоны.базаpptСавелий ЧепкасовОценок пока нет
- ГлюкозаДокумент9 страницГлюкозаbibibikОценок пока нет
- этилбензолДокумент34 страницыэтилбензолsaverma86Оценок пока нет
- PAAДокумент12 страницPAAVlados SmirovОценок пока нет
- Сложные эфиры. Жиры.Документ29 страницСложные эфиры. Жиры.jamosa2007Оценок пока нет
- BIOTECHДокумент19 страницBIOTECHbattaiza moakofiОценок пока нет
- Диагностический срез 11 классДокумент2 страницыДиагностический срез 11 классAlexandriks 101Оценок пока нет
- Угольная кислотаДокумент6 страницУгольная кислотаSonyaОценок пока нет
- Углеводы и липидыДокумент27 страницУглеводы и липидыGutОценок пока нет
- Biologija 7 FgosДокумент59 страницBiologija 7 FgosGenosse KommissarОценок пока нет
- Задачи. ХимияДокумент5 страницЗадачи. ХимияGenosse KommissarОценок пока нет
- Задание МОХДокумент5 страницЗадание МОХGenosse KommissarОценок пока нет
- Помощь ФредерикаДокумент6 страницПомощь ФредерикаGenosse KommissarОценок пока нет
- КомментаторДокумент2 страницыКомментаторGenosse KommissarОценок пока нет
- Specialnye Obrazovatelnye Uslovija Dlja Detej S ZaДокумент9 страницSpecialnye Obrazovatelnye Uslovija Dlja Detej S ZaGenosse KommissarОценок пока нет
- методика Копинг - стратегииДокумент6 страницметодика Копинг - стратегииGenosse KommissarОценок пока нет
- Магос 2.0Документ14 страницМагос 2.0Genosse KommissarОценок пока нет
- Отчёт ДементиюДокумент2 страницыОтчёт ДементиюGenosse KommissarОценок пока нет
- Книга МеханикусДокумент7 страницКнига МеханикусGenosse KommissarОценок пока нет
- Biologija 6Документ13 страницBiologija 6Genosse KommissarОценок пока нет
- Пригодится для диплома. ПроектыДокумент85 страницПригодится для диплома. ПроектыGenosse KommissarОценок пока нет
- Dioksiny Vysokaya Ekologicheskaya OpasnostДокумент3 страницыDioksiny Vysokaya Ekologicheskaya OpasnostGenosse KommissarОценок пока нет
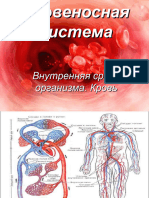
- Презентация по биологии - Кровеносная система -, 8 классДокумент44 страницыПрезентация по биологии - Кровеносная система -, 8 классGenosse KommissarОценок пока нет